注册登录才能更好的浏览或提问。
您需要 登录 才可以下载或查看,没有账号?立即注册
×
关键词:D-二聚体,深层静脉栓塞,POC床边检测,化学发光免疫测定
摘要:本文的目的为评估新的快速、定量PATHFAST D-二聚体检测诊断临床疑似深层静脉栓塞(DVT)患者的准确性指标。对82例疑似下肢深层静脉栓塞患者(34%患有DVT,66%无DVT),使用PATHFAST免疫分析仪进行D-二聚体(D-Dimer)检测。PATHFAST D-二聚体实验(以化学发光酶免疫测定原理为基础)的对于DVT的诊断价值利用预测临床发病率、加压超声成像(CUS)进行评估。此外,如果必要的话,每个患者要接受X线静脉造影与计算机层析成像。对于阳性诊断率(PPV)与阴性诊断率(NPV)分别为66.7%与100%的DVT诊断,使用0.570μg/mL FEU作为临床临界值的D-二聚体检测的灵敏度与特异性分别为100%与63.2%。PATHFAST D-二聚体与VIDAS D-二聚体结果间的相关性可接受(y=1.134×+0.003, r=0.902)。实验复现性良好(CV%:血浆4.0%-5.0%,全血7.1%-7.5%)总不精密度良好(CV%: 3.6-5.7%)。全血与血浆都可作为此实验样本(肝素化标本:y=1.013×-0.010,r=0.971;柠檬酸盐标本:y=1.068×+0.003, r=0.989)。由于其灵敏性较高,NPV PATHFAST D-二聚体实验可用于在疑似血栓患者中快速排除DVT。
? 2007 Elsevier Ltd. 版权所有.
引 言
疑似深层静脉栓塞(DVT)很常见,一个生命周期累积发病率为2-5%[1]。加压超声成像(CUS)与X线静脉造影是诊断DVT的最可靠的方法[2]。静脉造影是诊断DVT的金标准,但由于其造影剂引起的创伤与风险使其并不理想。CUS需要熟练的研究员,由于检查的下肢部位不同其灵敏度与特异性变化较大。
D-二聚体是一种交叉纤维素降解产物的混合物,是内源性纤维蛋白溶解的标志,因此可在DVT患者中检测出。回顾性研究指出为使用的检测考虑进一个界定临界值时,用于排除DVT的D-二聚体浓度的阴性诊断率较高[4] 。而且,大量研究证明D-二聚体检测结果阴性与超声波检测正常的患者的抗凝抑制作用安全[5,6] 。
一些D-二聚体检测,包括酶免疫测定、乳胶实验与免疫浊度实验目前都可利用,但它们的临床效率明显不同。其中,与乳胶实验相比较,检测DVT酶免疫测定的灵敏度与阴性诊断率(NPV)较高[7-13] 。一些实验可用于急诊床旁检测(POCT),其中VIDAS D-二聚体实验是DVT诊断或排除的惯用方法。新研发的PATHFAST D-二聚体实验是使用化学发光基质以酶免疫测定原理为基础的灵敏、定量方法。样本为全血与血浆,反应时间只有5分钟。我们进行此项研究的目的是评估使用D-二聚体实验作为筛查检测排除DVT时的诊断价值。
材料与方法
临床样本
此项研究包括82位门诊患者(40名女性,42名男性;年龄:23-85岁;女性:56.1±18.0岁,男性:46.8±17.7岁),涉及我们医院对疑似下肢DVT患者的诊断检查。28名患者诊断为DVT。符合下面任一条件的患者可排除:DVT既往病史,目前症状稳定或目前已进行过抗凝预防。肝素化或柠檬酸盐血液样本(数量=124;女性52,男性72;年龄:24-52岁)来自健康个体,这些个体是日本千叶市Mitsubishi Kagaku Iatron, Inc.的员工,他们已签署知情同意书。血液样本采集到10mL真空管内,里面含有0.129M枸椽酸钠或9IU锂肝素。全血样本在6小时内进行检测。为获得血浆样本,含有抗凝剂的血液样本在2000转/分下离心15分钟以获得缺乏血小板的血浆。血浆样本在6小时内检测或使用前在-40℃或-80℃冷冻储存。稳定性检测表明在-40℃或-80℃储存的样本至少可稳定3个月或更长时间。
深层静脉栓塞的诊断
我们研究所应用的DVT诊断检查以预测临床发病率(根据Wells等提出的得分) [14]与加压超声成像(CUS)(以标准为依据) [15]为基础。而且每个患者要进行X线静脉造影与计算机层析成像。
D-二聚体检测
PATHFAST? D-二聚体实验(Mitsubishi Kagaku Iatron, Inc.,东京,日本)是一种全自动、快速定量化学发光酶免疫测定,用来检测人全血与血浆样本中交叉纤维蛋白的降解产物(D-二聚体)。肝素与柠檬酸盐都可作为抗凝剂来获得血浆。PATHFAST免疫分析仪可通过样本辨识传感器自动区别全血与血浆样本。通过向PATHFAST免疫分析仪输入被检体的红细胞容积数值百分比,全血样本结果可任意修正。无数值调整时,PATHFAST免疫分析仪使用默认血细胞比容值(40%)。检测全血时,制造商建议全血样本分配到PATHFAST试剂盒样本槽后5分钟之内启动PATHFAST D-二聚体检测。PATHFAST D-二聚体实验是PATHFAST分析仪自动运行的一步式夹心免疫测定方法,可用即用试剂进行单一试验,包括共轭D-二聚体单克隆抗体的磁性颗粒与共轭D-二聚体单克隆抗体的碱性磷酸酶。Mitsubishi Kagaku Iatron, Inc.使用的D-二聚体抗体来自于交叉连接纤维蛋白的降解产物,作为免疫原。被胞浆素吸收后,抗体能够辨识交叉连接纤维蛋白降解产物的新生抗原。血液样本中D-二聚体抗原与试剂的免疫反应为5分钟,期间形成免疫复合物,Magtration?程序执行捕获/自由分离。在免疫复合物中添加化学发光基质(CDP-Star?)后检测化学发光信号。
实验的检测范围为0.005至5.00μg/mL FEU(纤维蛋白原等价单位),使用PATHFAST免疫分析仪检测血液样本17分钟后可读取最终结果。PATHFAST免疫分析仪一次运转可检测6个样本。
PATHFAST D-二聚体检测的批间重复性使用两组新鲜肝素化全血和血浆样本测定,分布含正常和不正常浓度的D-二聚体。检测批间重复性(n=20)的实验可在同一工作日进行。在20个不同的工作日,使用三组含正常和不正常浓度的D-二聚体的肝素化血浆样本评估总不精密度。
统计分析
通过绘制灵敏性数值对比1-特异性的值,建立受试者操作特性(ROC)曲线,然后计算曲线下面积(AUC)。使用ROC曲线的结果测定最佳D-二聚体临界值。根据范围的标准方法计算D-二聚体实验的灵敏性、特异性、阳性与阴性诊断率。根据二项式分布计算95%的置信区间(CI)。根据Spearman 计算相关性,使用Passing与Bablok方法进行回归分析[16]。
对比方法
此项研究使用Biomerieux VIDAS? D-二聚体试验[17]作为对比方法。根据制造商的使用说明进行试验。VIDAS D-二聚体试验是一种酶免疫测定,其检测范围为45ng/mL FEU(0.045μg/mL FEU),实验范围上限为10,000ng/mL FEU(10μg/mL FEU)。实验使用的临界值为500ng/mL FEU (0.500μg/mL FEU)。
结 果
PATHFAST D-二聚体的实验性能
PATHFAST D-二聚体实验的批间再现性与总不精密度见表1。D-二聚体不同浓度的两种样本的PATHFAST D-二聚体检测的批间再现性良好(CV%:正常浓度样本,血浆=5.0%,全血7.5%;不正常浓度样本,血浆=4.0%,全血7.1%)。PATHFAST D-二聚体检测的总不精密度可接受(CV%:正常浓度样本=4.1%,不正常浓度样本=3.6-5.7%)。
表一 PATHFAST D-二聚体检测的批间再现性与总不精密度
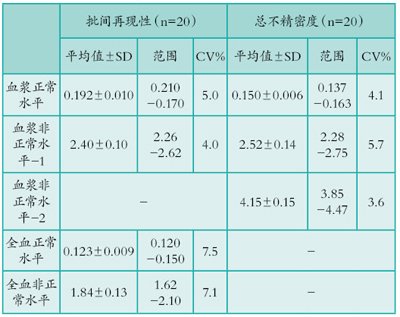
CV%,变异系数
参考数值
PATHFAST D-二聚体实验的参考区间来自健康志愿者(n=124)的枸橼酸钠血浆样本。D-二聚体浓度中间值为0.225μg/mL FEU,最高检测浓度为0.710μg/mL FEU。95%的参考上限为0.528μg/mL FEU。此结果支持研究中PATHFAST D-二聚体实验的暂定临床临界值(0.570μg/mL FEU)有效。
患者样本结果
对82名患者(40名女性,42名男性:年龄23-85岁;34%患有DVT)进行分析。如图1所示,得到的ROC曲线显示了PATHFAST D-二聚体实验在不同临界值下曲线面积为0.957(95% CI: 0.918-0.996)时的灵敏度与特异性数值。参考ROC曲线与参考区间的数值建立PATHFAST D-二聚体实验的临床临界值0.570μg/mL FEU。检测水平大约为0.570μg/mL FEU的PATHFAST D-二聚体实验的总不精密度为5%,良好。PATHFAST D-二聚体实验的灵敏度、特异性、阳性与阴性诊断率的分布见表2。正如所预料,使用较高的临界值(1.50μg/mL FEU),相应的灵敏度较低(92.9%),阴性诊断率较低(94.3%),特异性较高(86.8%)。
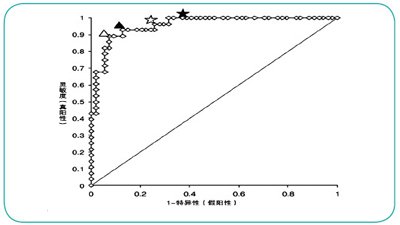
图1:PATHFAST D-二聚体实验检测深层静脉血栓准确性指数的受试者操作特性(ROC)曲线分析,(★)说明临界值为0.570μg/mL FEU,(☆)为0.800μg/mL FEU,(▲)为1.28μg/mL FEU,(△)为1.50μg/mL FEU。
全血与血浆的相关性
PATHFAST D-二聚体实验中使用的全血与血浆的D-二聚体结果的相容性见图2。D-二聚体抗原浓度正常与非正常的血液样本使用柠檬酸钠或肝素锂作为抗凝剂。线性回归分析得到的斜率为肝素1.013(95% CI: 0.931-1.063;x轴血浆,y轴全血;n=40),柠檬酸1.068(95% CI: 1.030-1.112;x轴血浆,y轴全血;数量=56),y截距为肝素-0.010μg/mL FEU (95% CI: -0.055至0.089),柠檬酸0.003μg/mL FEU(95% CI: -0.005至0.011)。相关系数为肝素与柠檬酸分别是0.971与0.989。
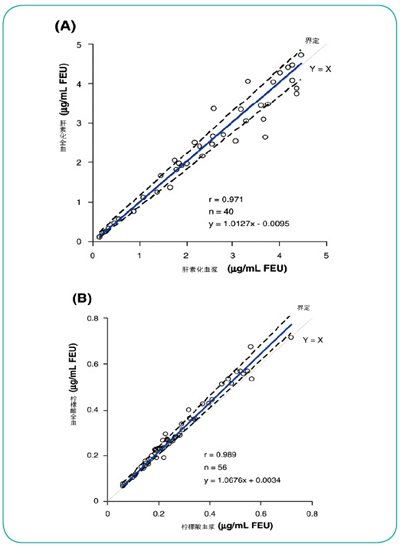
图2:PATHFAST应用血浆与全血所得结果的相关性。(A)肝素血液样本的D-二聚体浓度升高。(B)柠檬酸钠血液样本的D-二聚体浓度正常。
肝素全血与柠檬酸全血的相关性
使用来自健康个体的58例血浆样本,PATHFAST D-二聚体实验对比肝素化全血与柠檬酸全血的D-二聚体结果。线性回归分析得到的斜率为0.952(95% CI: 0.926-0.981;x轴,肝素;y轴柠檬酸),y截距0.001μg/mL FEU(95% CI: -0.005至0.006)。相关系数为0.995。
表二 PATHFAST D-二聚体检测排除DVT的临床性能
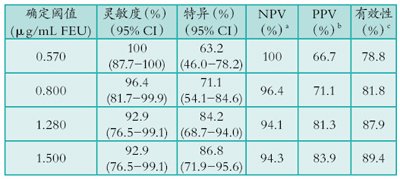
a NPV,阴性诊断率
b PPV,阳性诊断率
C 根据真阳性与真阴性总和除以结果的数量来计算。
方法对比
PATHFAST D-二聚体实验所得的结果与生物梅里埃 VIDAS D-二聚体实验的结果相比较,使用来自于住院患者与健康个体的柠檬酸血浆样本。PATHFAST D-二聚体实验与VIDAS实验(n=66)的结果之间非常显著的相关性见图3。PATHFAST D-二聚体实验与VIDAS实验结果的相关系数为0.902,回归线显示y截距为0.0025μg/mL FEU(95% CI: -0.125至0.087),斜率为1.134 (95% CI: 1.030-1.329)。VIDAS D-二聚体实验的临床临界值为500ng/mL FEU(0.500 μg/mL FEU)。
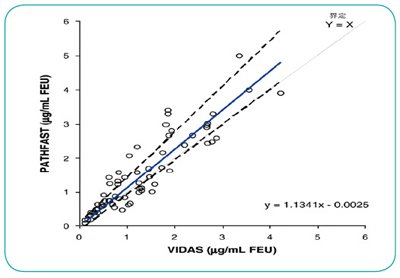
图3:PATHFAST D-二聚体与VIDAS D-二聚体结果的相关性。
讨 论
此项研究的目的为评估PATHFAST D-二聚体实验的技术参数与诊断功能。使用ROC曲线分析建立临床D-二聚体临界值,研究实验的灵敏度、特异性、NPV与PPV。
20世纪80年代以来便应用D-二聚体检测辅助排除DVT。在健康个体的D-二聚体上限值的批内再现性还有总不精密度起着很重要的作用,因为在此水平不精密度较高可引起假阴性结果。使用PATHFAST D-二聚体检测,低浓度与高浓度D-二聚体(批内:血浆CV =4.0%,全血CV=7.1%;总不精密度:血浆CV=3.6-5.7%)都能得到良好的批内再现性(血浆CV=5.0%,全血CV=7.5%)和总不精密度(血浆CV=4.1%)。这些参数证明PATHFAST D-二聚体实验是一种准确、定量的方法,尽管其使用POC台式分析仪。
为排除DVT,准确性、较高的灵敏度与NPV对D-二聚体实验都非常重要。D-二聚体敏感性实验由于其非特异性有时会受到质疑,产生大量阳性结果,因此需要进一步的研究以确定最终的诊断结果。但是这需要考虑敏感性方法的临界值可自由选择。特别在与临床发病率评估共同应用时,通常选择较高的临界值来强化实验的特异性,从而在大量患者中排除DVT [19]。
研究中我们观察PATHFAST D-二聚体实验的灵敏度与NPV并分析ROC曲线,这说明此检测可作为排除DVT的重要工具而应用。总之,虽然阴性结果数量较低使其在临床应用中的价值较低,但降低此实验的临界值可提高灵敏度。临界值设定为0.570μg/mL FEU,PATHFAST D-二聚体实验的特异性与PPV分别为63.2%与66.7%。将这些结果与前面所描述的VIDAS D-二聚体实验结果相比较[20,21]。以此项研究结果为基础,确定0.570μg/mL FEU浓度为PATHFAST D-二聚体检测的临床临界值,因为此数值的灵敏度为100%,但排除DVT也要考虑健康个体的参考上限0.528μg/mL FEU。
即使未纠正血细胞比容值,PATHFAST D-二聚体实验使用全血与血浆样本所得结果的可比性仍可接受。每个全血结果都使用各自血细胞比容值的百分比(数据未显示)纠正,会略微增加全血与血浆间的相关性。尽管使用的柠檬酸全血样本的血细胞比容值范围为29.3至49.9%(平均值±SD=40.8±3.8),对于围绕临床临界值(PATHFAST D-二聚体实验0.570μg/mL FEU)的全血样本未纠正血细胞比容值的情况下,对比研究显示全血与血浆的相关性良好。通过向系统中输入非正常血细胞比容值样本(如红细胞增多症和严重贫血症病人的样本)各自的血细胞比容值,PATHFAST分析仪也可将每个全血的结果纠正为血浆D-二聚体浓度。
如图3所示,PATHFAST D-二聚体实验与VIDAS D-二聚体实验间的对比方法说明两个D-二聚体实验的相关性良好。Watanabe【22】等指出VIDAS D-二聚体实验排除日本患者的DVT,建立的临床临界值为0.6μg/mL FEU。这个结果可与PATHFAST D-二聚体实验的结果相比较。
总之,新型定量5分钟D-二聚体实验——PATHFAST D-二聚体与潜伏期计数检查相结合是临床医生排除DVT的有价值的方法。此项研究的灵敏度与NPV较高,因此PATHFAST D-二聚体检测有可能作为独立试验应用。但仍需要进一步应用大量患者进行研究,以更好的确定其用于排除DVT的临床临界值,并确认该方法在D-二聚体浓度低于临界值的抗凝治疗的患者中的潜在用途。
致谢
PATHFAST D-二聚体试剂由日本东京的Mitsubishi Kagaku Iatron, Inc.提供。
参考文献
[1] Wells PS, Anderson DR, Rodger M, Forgie M, Kearon C, Dreyer J, et al. Evaluation of D-Dimer in the diagnosis of suspected deep-vein thrombosis. N Engl J Med 2003;25:1227-35.
[2] Stephen JM, Feied CF. Venous thrombosis, symposium. Postgrad Med 1995;97:36-47.
[3] Ricotta S, Iorio A, Parise P, Nenci GG, Agnelli G. Post discharge clinically overt venous thromboembolism in orthopaedic surgery patients with negative venography — an overview analysis. Thromb Haemost 1996;76:887-92.
[4] Bounameaux H, De Moerloose P, Perrier A, Miron MJ. DDimer testing in suspected venous thromboembolism: an update. Q J Med 1997;90:437-42.
[5] Bernardi E, Prandoni P, Lensing AW, Agnelli G, Guazzaloca G, Scannapieco G, et al. D-Dimer testing as an adjunct to ultrasonography in patients with clinically suspected deep vein thrombosis: prospective cohort study. The Multicentre Italian D-Dimer Ultrasound Study Investigators Group. BMJ 1998;317:1037-40.
[6] Kraaijenhagen RA, Piovella F, Bernardi E, Verlato F, Beckers EA, Koopman MM, et al. Simplification of the diagnostic management of suspected deep vein thrombosis. Arch Intern Med 2002;162:907-11.
[7] Charles LA, Edwards T, Macik GB. Evaluation of sensitivity and specificity of six D-dimer latex assays. Arch Pathol Lab
Med 1994;118:1102-5.
[8] Freyburger G, Trillaud H, Labrouche S, Gauthier P, Javorschi S, Bernard P, et al. D-dimer strategy in thrombosis exclusion. Thromb Haemost 1998;79:32-7.
[9] Elias A, Aptel I, Huc B, Chale JJ, Nguyen F, Cambus JP, et al. D-dimer test and diagnosis of deep vein thrombosis: a comparative study of 7 assays. Thromb Haemost 1996;76: 518-22.
[10] Tardy B, Tardy-Poncet B, Viallon A, Lafond P, Page Y, Venet C, et al. Evaluation of D-dimer ELISA test in elderly patients with suspected pulmonary embolism. Thromb Haemost 1998;79:38-41.
[11] Legnani C, Pancani C, Palareti G, Guazzaloca G, Fortunato G, Grauso F, et al. Comparison of new rapid methods for Ddimer measurement to exclude deep vein thrombosis in symptomatic outpatients. Blood Coagul Fibrinolysis 1997;8:296 302.
[12] Scarano L, Bernardi E, Prandoni P, Sardella C, Rossi L, Carraro P, et al. Accuracy of two newly described D-Dimer tests in patients with suspected deep venous thrombosis. Thromb Res 1997;86:93-9.
[13] Stein PD, Hull RD, Patel KC, Olson RE, GhaliWA, Brant R, Biel RK, et al. D-Dimer for the exclusion of acute venous thrombosis and pulmonary embolism. Ann Intern Med 2004;140:589-602.
[14] Wells PS, Anderson DR, Bormanis J, Guy F, Mitchell M, Gray F, et al. Value of assessment of pretest probability of deep-vein thrombosis in clinical management. Lancet 1997;350:1795-8.
[15] Lensing AWA, Prandoni P, Brandjes D, Huisman PM, Vigo M, Tomasella G, et al. Detection of deep-vein thrombosis by real-time B-mode ultrasonography. N Engl J Med 1989;320: 342-5.
[16] Eisenwiener HG, Bablok W, Bardorff W, Bender R, Markowetz D, Passing H, et al. Statistical Auswertung beim Methodenvergleich. Lab Med 1984;8:232-44.
[17] VIDAS package insert. VIDAS - D-Dimer New (DD2). REF 30 442 2003/09; 008120-4.
[18] Becker DM, Philbrick JT, Bachhuber TL, Humphries JE. Ddimer testing and acute venous thromboembolism. A shortcut to accurate diagnosis? Arch Intern Med 1996;156: 939-46.
[19] von Lode P, Rainaho J, Liaho MK, Punnonen K, Peltola O, Harjola V-P, et al. Sensitive and quantitative, 10-min immunofluorometric assay for D-Dimer in whole blood. Thromb Res 2006;118(5):573-85.
[20] Legnani C, Fariselli S, Cini M, Oca G, Abate C, Palareti G. A new rapid bedside assay for quantitative testing of D-Dimer (Cardiac D-Dimer) in the diagnostic work-up for deep vein thrombosis. Thromb Res 2003;111:149-53.
[21] Waser G, Kathriner S, Wuillemin WA. Performance of the automated and rapid STA Liatest D-dimer on the STA-R analyzer. Thromb Res 2005;116:165-70.
[22] Watanabe R, Wada H, Mori Y, Nakasaki T, Sawa H, Shiku H. Plasma D-dimer levels in patients with deep vein thrombosis. Rinsho Byori 1999;47:887-90 (in Japanese).
|