[摘要]
目的 为用于排除静脉栓塞疾病(VTE)的D-二聚体检测指南检测提供指南。
方法 主要参考美国临床和实验室标准化研究院(CLSI)H47-A2文件相关内容,并结合具体的实际进行总结。
结果 D-二聚体的阴性值有利于排除静脉栓塞。正确使用D-二聚体的值需要对VTE的临床决定预测概率进行描述,正确采集和处理标本,确定排除VTE的阈值以及正确解读检测结果。
结论 对D-二聚体的检测对于临床评价静脉栓塞疾病具有重要的意义。在实际工作中要紧密联系临床,严格按照操作规程和厂家说明,保证结果的准确可靠,为临床提供诊疗依据。
[关键词] D-二聚体检测;静脉栓塞;阴性预测值;纤维蛋白降解产物
1 D-二聚体检测概述
1972年,尽管当时交联纤维衍生物(一种纤维蛋白在体内形成和降解的标志)的检测需要使用聚丙烯凝胶电泳,不适合于临床常规检测。但人们仍预测其检测将成为一个有用的诊断工具。第二年,发现了人类纤维蛋白经纤溶酶水解作用之后产生的一种独特的降解片段,即D-二聚体。十年后,文献报道了一种使用单克隆抗体的对低浓度D-二聚体敏感的固相酶免疫检测方法。之后不久,又有两个研究团队报道了在肺栓塞(PE)、深静脉血栓(DVT)、弥散性血管内凝血(DIC)和动脉血栓的患者中D-二聚体浓度增高。在过去的十年里,发表了多篇研究确认D-二聚体水平在急性静脉栓塞(VTE)的患者体内增高,如果其浓度低于已建立的阈值则可排除这种情况。
1.1 静脉栓塞的背景
静脉栓塞(VTE)可能会产生严重的甚至危及生命的后果。最常见的静脉栓塞疾病是下肢深静脉血栓(DVT)和肺栓塞(PE)人群中静脉血栓的发病率是1/1000每年,75岁及以上的人群的发病率升高了1/100。年龄较低的人群发病率较低,15岁到49岁的健康女性静脉栓塞的发病率在1/10000左右。静脉栓塞的治疗是使用抗凝剂和维生素K拮抗剂,在3~6个月的治疗期内有2%的出血风险和0.5~1%的死亡率。因此只对有客观患病证据的患者进行抗凝剂治疗。
仅仅基于临床上的发现对于静脉栓塞的诊断是不可靠的,在诊断前进行客观的检查是必要的。非侵入性影像技术的发展和诊断不确定度的要求更严格使得进行影像学检查的可疑的静脉栓塞患者数量增加。经过影像学检查后,可疑患者中只有15~25%确认为静脉栓塞,因此静脉栓塞的患病率只有5%。尽管静脉超声是一种非侵入诊断技术,但是对大部分患者进行超声检查费钱费力,而且90%的患者没有静脉栓塞。影像分析对于PE的诊断也有局限。肺通气-灌注扫描是临床上最常用的方法,但是也只能诊断20~30%的病例;肺血管造影是诊断PE的金标准,但是也有0.5%的死亡率和1%的重大并发症。斜螺旋计算机断层扫描是最近引进的PE检测方法,研究显示可安全的取代通气灌注扫描和肺血管造影,安全诊断和排除PE,但是这项检测成本较高。鉴于上述原因,需要一种灵敏、廉价、非侵入的检测方法。若D-二聚体检测用于静脉栓塞诊断的阈值已得到建立和确认,D-二聚体检测与标准的验前概率(PTP)结合,可成功用于排除静脉栓塞,且不需要影像诊断。
1.2 D-二聚体检测
D-二聚体是指交联的纤维蛋白(原)降解产物(FDP)的混合物,每一个FDP含有一个或数个D-D结构域。为了使实验室能够使用这种方法来检测血凝块的构象和溶解以排除静脉栓塞的存在,这项检测必须足够敏感。当使用较高阴性预测值(NPV)的检测时,得到低于预先设定阈值的结果则提示不存在临床上有意义的血栓。在诊断静脉栓塞方面,D-二聚体的NPV具有很大的价值。阴性的D-二聚D-二聚体值可排除静脉栓塞的存在。研究显示敏感的阴性D-二聚体检测可排除高达30%的栓塞事件。随着检测人群患病率的增加,假阴性概率也会增加,因此,不要使用定量的D-二聚体检测排除阳性预测值较高的静脉栓塞患者。
作为纤维蛋白溶解产物,D-二聚体水平在其他病理条件下也可能增高如:弥散性血管内凝血DIC、败血症、恶性肿瘤、炎症、外伤或手术。随着年龄或者正常妊娠而增加。本文中讨论的定量D-二聚体检测只用于排除低或中度PTP的静脉栓塞疾病。很多D-二聚体检测方法快速、简单、廉价(相对于影像检查的成本),且有较高的灵敏度和对静脉栓塞有较高的NPV值。可靠的阈值对于检测结果的解释是必须的,低于这个阈值的检测结果对静脉栓塞诊断有较高的NPV值。但是,尽管D-二聚体检测已经得到了广泛的应用,很多临床医生对不同方法得到的不同检测结果的数值、单位和阈值感到困惑。
1.3 D-二聚体检测存在的问题
纤维蛋白D-二聚体是交联纤维蛋白最小的交联讲解产物。但是针对D-二聚体的单克隆抗体同时对交联纤维蛋白和各种交联FDPs。尽管D-二聚体片段是D-二聚体特异性抗原的单克隆抗体检测的最小单位,实际上,单克隆抗体检测含有这个抗原的各中FDPs。临床标本一般含有不同量的D-二聚体片段和高分子量胶原FDPs。不同抗体对这些产物对这些产物有不同的特异性,有些优先结合到高分子量交联产物,有些优先结合到低分子量片段。除了抗体选择外,检测原理(比浊、ELISA或其他方法)也与D-二聚体产物的不同敏感性有关。FDPs的交联活性可能是某种检测方法的局限,但是这个问题不会对静脉栓塞的排除造成影响。
1.4 协调与标准化
D-二聚体 缺乏标准化是一个问题,其中主要的原因是D-二聚体检测缺乏国际参考品(IRP)。用市场上各种含有D-二聚体分子的生物学材料来制备IRP是复杂的,因为这些材料不能近似于(纯的)纤维蛋白片段的混合物。厂家一般选用校准物来反映他们的检测需要,而不是使D-二聚体检测具有可比性。校准材料可能含有纯化的D-二聚体片段、半纯化高分子量交联纤维蛋白产物,或者混合的血浆样本。校准物的机制可能是缓冲液或者添加了血浆、血清、纤维蛋白或其他人或动物来源的缓冲液。
最开始尝试用纯化的D-二聚体片段作为校准物使D-二聚体检测标准化。由于不同试剂盒的抗体不同,并不是所有的抗体都能够识别D-二聚体,因此这种方法不可行。同时,有些乳胶凝集检测不能使用这些小片段交联。在开始的时候,认为D-二聚体的标准化是不可行的,因此开始尝试使用稳态被打乱的患者血浆样本协调检测。这些研究表明了临床样本比纯化的FDPs具有较小的检测间的变异,反映了临床样本中交联产物的异质性。在检测高浓度D-二聚体的混合患者标本浓度时,各方法间表现出最佳一致性。使用这个方法,所有方法的D-二聚体公议值与特殊方法所得的比值可得到一个转化因子,用其来表示不同检测方法简单协调程度。但是在高低浓度范围内还是存在较大的差异。
Meijer等人将高浓度的患者血浆与正常人浓度血浆混合制备了5份不同浓度的样本。将这5个浓度水平的标本分发到500过个实验室,用所得数据计算了每个浓度水平的中位数作为参考线,以及方法特异的回归线。将方法特异的回归线转化成参考线从而实现方法间的协调。用这种模型可以显著减少方法间的变异,作者建议厂家应该对其校准物进行协调。尽管这种方法很值得推荐,但是还是存在一些问题:研究只协调了欧洲制造的7中检测方法,其他的新的检测方法可能会造成参考线的漂移;还是存在厂家校准物组成的差异;要不断获得所需体积的患者标本体积存在困难。
考虑到这些局限,建议使用含有与临床标本具有相似浓度范围的交联FDPs体外制备物作为参考物质。理想的参考物质可能含有较高的D-二聚体水平,且不含病毒或病毒激活的。所含的真正的D-二聚体通过进行最终的纤溶酶消化得到确认,以使高分子量产物中所含的所有D-二聚体抗原都降解成了D-二聚体片段。当制备了适当的IRP时,厂家采用它才有可能实现D-二聚体的标准化。到目前为止,协调是最有可能解决单位和阈值设定问题的方法。
2 患者评估和预测概率
包括D-二聚体在内,没有哪一项单独的检测有足够的敏感度和特异度可以诊断或排除静脉栓塞的可疑患者。但D-二聚体与其他诊断或临床评估模式结合,其对诊断静脉栓塞具有重大意义。
静脉栓塞不能单纯通过临床评估进行诊断,主要是深静脉栓塞和肺栓塞的临床症状和体征是非特异的。尽管静脉栓塞不能在临床基础上准确诊断,但是临床医生可以正确的将患者分成VTE可能,VTE不可能,或者VTE概率低、中、高。准确确定疾病的可能性(阳性预测值)可以通过标准化的评分系统来实现,所用的评分系统是从大型数据库得到的标准和危险因素的基础上建立的,见表1和2。所列的标准化预测规则已被推荐用于临床评价PE和DVT的概率。这些标本已在临床试验中得到了确认,用于其它人群也是可靠的。
将临床评价规则与D-二聚体检测联合确定患者VTE的可能性比单独使用其中之一评价栓塞更可靠。将定量D-二聚体在确定阴性预测值时发挥了最大作用,它可用于将患者分成“不可能”、“低-中”临床概率。这些患者的诊断取决于D-二聚体检测的NPV值,若D-二聚体的值低于排除阈值则提示没有静脉栓塞,静脉栓塞的诊断可以有把握的排除且没有必要进行进一步的影像学检查。当静脉栓塞的临床概率高(或可能),D-二聚体检测不能够提供足够的信息,应该进行合适的影像学检查,例如下肢超声、通气灌注扫描或者螺旋CT。当临床概率落到了低或中度范围内,排除静脉栓塞取决于D-二聚体检测的NPV值。当D-二聚体的阈值设置的太低,甚至是正常水平,健康个体不能被排除。当D-二聚体检测敏感度有限,且阈值太高,则会漏诊。
表1 DTV可能性判断(Wells评分)
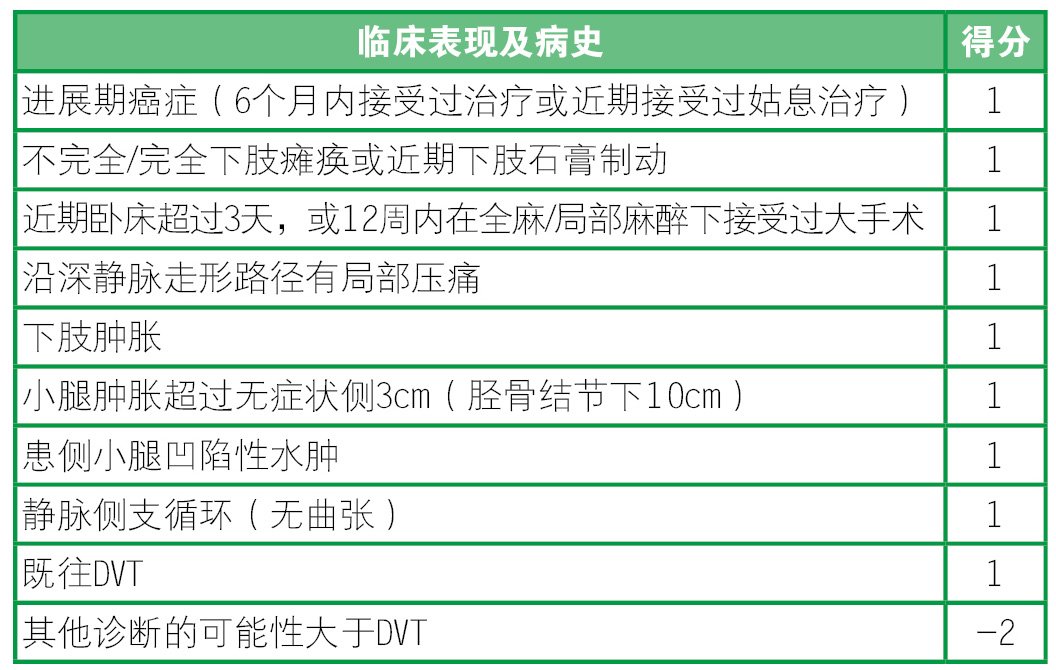
DTV危险分层:低度危险 :≤0分;中度危险:1~2分;
高度危险:≥3分
DTV临床可能性:不可能:<2;可能≥2
只有在Wells得分<2时,D-二聚体检测用于排除DTV
表2肺栓塞预测概率:比较Geneva和Wells评分
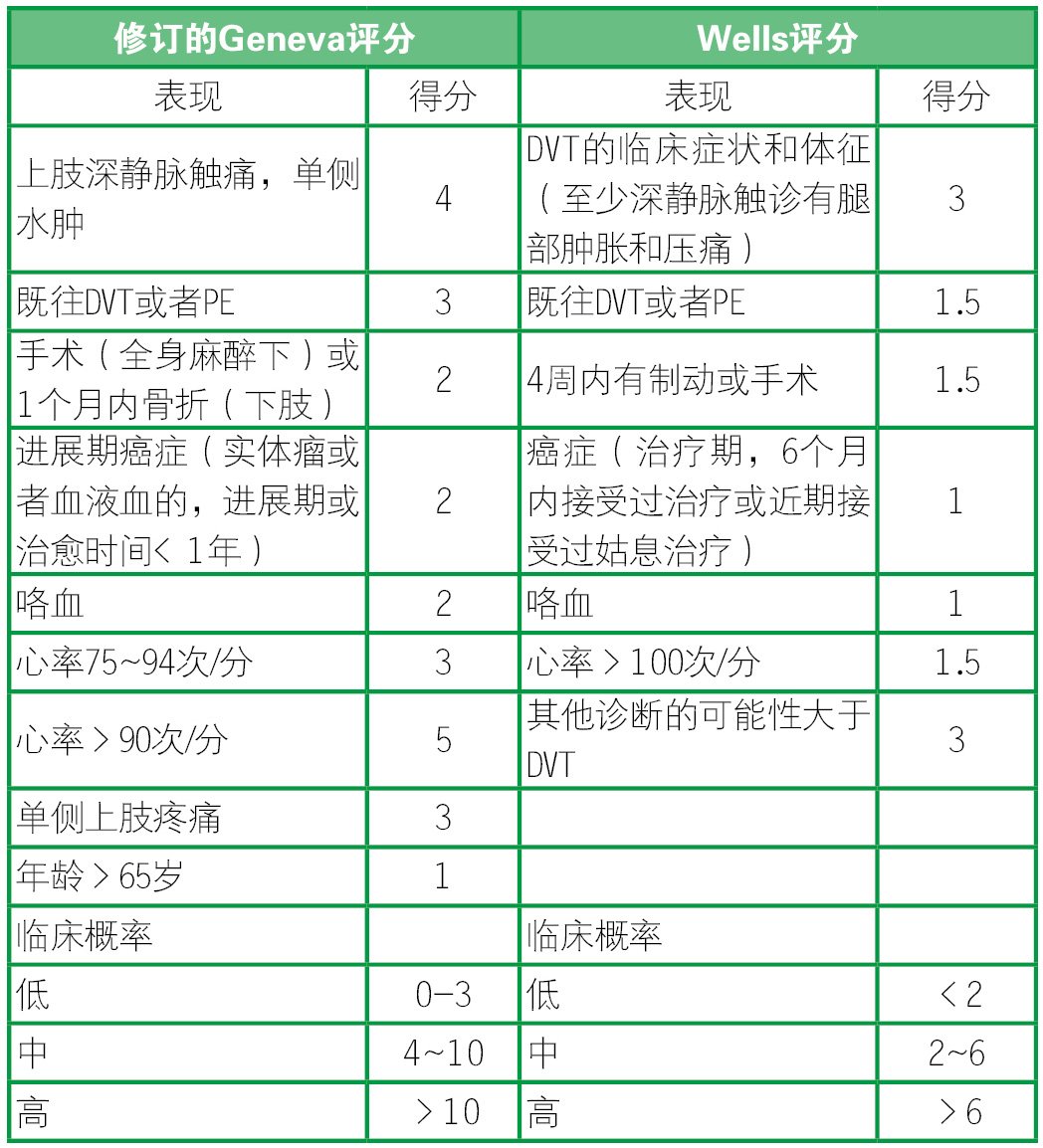
仅当Geneva得分<10分时,用D-二聚体排除PE;仅当Wells得分<6分时,用D-二聚体排除PE。
2.1与患者状态或治疗有关的局限性
以下是与栓塞发生无关的可能影响D-二聚体水平的患者状态和治疗。7天内进行纤溶治疗;4周内外伤或手术;大血肿;浸润癌;败血症,严重感染,肺炎;肝硬化;妊娠;动脉粥样硬化;镰刀红细胞贫血;高龄。
D-二聚体检测可能会出现假阴性,例如在检测前开始了24小时或更长时间的抗凝治疗。抗凝治疗可能导致浓度的降低,从而出现假阴性。因此,用于排除静脉栓塞或PE时,D-二聚体不能用于进行抗凝治疗的患者的辅助诊断。其次,当血凝块较小时不足以使D-二聚体浓度超过阈值。这种情况更有可能出现在血块从末端到膝盖,一般在腿的深静脉的三叉处,减小了静脉的口径。如果血块是从末端到膝盖,D-二聚体检测不能用于排除下肢静脉DVT。此外,小的肺栓塞可能不能是D-二聚体的检测结果超过排除PE的阈值。由于这个原因,D-二聚体检测不适合用于排除上肢静脉栓塞(UEDVT),因为UEDVT的值显著低于下肢静脉DVT。如果从栓塞发生到检测的时间过长,也有可能由于D-二聚体在循环过程中被清除而低于阈值。这个时间的长短与血块的大小有关。小的血块从发生到检测低于阈值的时间较短。在少数情况下也可能由于组织型纤溶酶原激活物不足,D-二聚体的水平低于阈值造成假阴性。D-二聚体检测阴性但是存在凝血块的情况也可能是影像学的假阳性。最后,不推荐对儿童使用定量D-二聚体检测排除VTE。在以发表的文献中,15%的肺栓塞儿童的D-二聚体值正常。由于这种原因,预测概率得分,例如PE的Wells简化概率得分,不能像用于成年人一样用于儿童。
3.标本采集和处理
密切监测D-二聚体检测前患者的临床情况以确保结果能够反映患者的真实状态。
3.1患者的情况和标本采集前准备
血浆中可测量的D-二聚体的水平取决于血栓的大小和形成时间。D-二聚体可在血栓形成后2个小时内检测到。D-二聚体的半衰期大概是7个小时,这有助于解释患者在一定时间内连续检测的结果。D-二聚体的半衰期同样也与排除VTE的检测灵敏度有关,血栓形成到检测的时间越长灵敏度越低。患者在出现VTE症状之后的数周到数月检测的D-二聚体值低于阈值的可能性可能比一发现症状马上检测的概率要大得多。接受抗凝治疗患者的D-二聚体排除VT的灵敏度会降低。这种情况下,很可能会发生假阴性。大手术后,D-二聚体值身高,7天达到峰值,接着以每天6%的速度清除,保持4周或以上的升高时间,取决于手术的情况。
3.2标本采集
D-二聚体检测的标本使用真空试管系统或者注射器采集。按照所用的检测方法选择全血标本或值血浆标本。D-二聚体检测所含的抗体不与纤维蛋白原反应,血浆是适当的标本类型。检测血浆的大部分商业检测方法需要枸橼酸钠抗凝血浆。从实际的角度考虑,一般推荐按照CLSI H21关于标本采集的规定,这个指南详细说明了红细胞比容升高、真空试管中标本过多或过少的情况处理,推荐的枸橼酸钠浓度,用植入式血管装置采集标本的正确流程。按照厂家推荐的方法采集静脉血,通常抗凝的枸橼酸三钠的浓度是109 mmol/L (3.2%) 和 129 mmol/L (3.8%),使得抗凝剂与血标本的比例为1:9(推荐度额枸橼酸三钠的浓度为109mmol/L)。
在某些D-二聚体检测方法中,结果不会受到抗凝剂的影响,可以使用枸橼酸钠、EDTA或者肝素。具体选用哪种抗凝剂要根据检测系统而定。特别是如果使用床旁检测(POC)仪器,EDTA抗凝标本可用全血或者EDTA血浆。有些POC仪器只能用肝素抗凝的全血。
D-二聚体标本采集不必要使用一次性试管。在采血过程中药避免淤血或损伤,这些可能导致D-二聚体的水平升高。如果使用真空装置,标本的量要正确。凝血是标本拒收的原因之一。
3.3标本处理、运送和保存
乳糜血和溶血标本可能会对检测造成干扰,特别是对于定量、微粒凝集检测。干扰的大小取决于所用光的波长和乳糜血和溶血的程度。厂家说明中应该包含干扰的相关数据。如果认为标本可接受,将标本稀释可减少干扰。标本中较高的类风湿因子可能对某些微粒凝集免疫检测造成干扰。但是,商品化的D-二聚体检测声称类风湿因子对离子检测没有干扰。
嗜异性抗体尽管很少见,但是它的存在会影响商品化的检测,因为试剂中存在动物来源的单克隆或者多克隆抗体。这种现象可见于冷沉淀球蛋白血症。对于这种标本,可以用含大量未免疫过的动物抗体的方法学以减少嗜异性抗体的干扰,详见CLSI I/LA30。商品化的产品对样本进行了预处理,在检测前去除了嗜异性抗体。这种产品一般用于化学实验室,但是对于含有嗜异性抗体的患者并不适用。适用这种试剂可能与某些反应试剂不相容,因此需要确认。
4 检测方法学
选择D-二聚体检测方法排除VTE时,评价检测的灵敏度和NPV是非常重要的。试剂盒或方法的选择还应该考虑以下方面:定量还是定性,出结果的时间,是否可在任意时间检测标本(如批量检测可能会延长结果报告时间),结果报告用的单位:FEU、DDU、纳克每毫升、微克每升、微克每毫升或毫克每升,结果报告的诊断阈值:厂家建立或者自己建立,预期目的:排除诊断或者辅助诊断,临床安全性:非侵入性的、时间成本效益。
4.1定量夹心检测
定量夹心检测可分为ELISA和非ELISA检测两类。用于D-二聚体检测的ELISA方法是夹心ELISA。捕获D-二聚体的特异性抗体包被在固相载体上,如聚苯乙烯试管或者微孔板。检测抗体与D-二聚体的相同或者不同位点结合,抗体与酶结合作为信号产生系统。根据检测抗体的特异性,两个抗体与样本所含抗原结合,形成一个或多个二聚体结构域。以上结合可通过一或两步实现。两步法过程中,添加检测抗体前先洗去未反应的样本。反应后第二次洗去多余的检测抗体。根据不同的底物,可产生显色、荧光或者化学发光信号并测量。信号强度与存在的D-二聚体的量成比例。
ELISA检测因固相载体、抗体和信号产生系统的不同而有差异。自动化的均相检测有很多常用的固相如与膜结合的聚苯乙烯头、珠子、聚合物或微粒子,如径向分离免疫测定法(RPIAs) 和磁性微粒子免疫测定法(MIAs)。在孵育阶段,聚合物、微粒子和微米大小的粒子处于悬浮状态。分子弥散距离减少,加速了反应。含有4-甲基伞花基磷酸盐的碱性磷酸盐(酶联荧光测定ELFA)或者作为信号产生系统。其他系统使用丫啶酯、4-氨基邻苯二甲酰肼或黄胺直接产生化学发光信号,不需要酶促反应。
4.2定量微粒子凝集
微粒子凝集是均相免疫测定,常用于D-二聚体检测。均相免疫测定只需要混合样本和免疫化学试剂,然后检测。免疫化学试剂结合产生可检测的物理信号,不需要分离结合物质与游离物质。微粒子产生的光散射强度取决于粒子的大小。因此,随着反应的进行免疫化学反应产生的微粒子凝集改变了光散射的量。对于定量D-二聚体检测,适宜使用直径在0.1~0.5μm的聚苯乙烯粒子。粒子上包被1~2种特异抗体。凝集反应通过透射比浊或散射比浊来测定。透射比浊测量一束光线透过标本后的强度。散射比浊是关线经标本散射后与原始光线方向成一定角度收集到的光强度。微粒减少由于标本中粒子物质存在的干扰,要检测加入标本后的吸光度改变。加上离心这个检测过程不到10分钟,可在常规实验室的自动分析仪和凝血仪上应用。
4.3半定量微粒子凝集方法
旧的D-二聚体检测方法是手工半定量乳胶或红细胞凝集方法。尽管这些检测对于检测大量的循环D-二聚体如DIC、血栓溶解或其他条件,对于排除VTE来说太敏感。这些检测一般是通过将患者标本与抗体包被的乳胶珠子或者检测卡上的红细胞混合。如果D-二聚体水平显著升高,出现凝集,造成可见的凝集。得到的玻片通过技术人员用显微镜来确定是否存在凝集。这些检测的有较高的观察者间的终点判断变异。目前的研究不支持用这些检测来排除VTE。
4.4床旁检测
当需要定量方法学或结果但缺乏自动化定量的检测仪器时,小型实验室可以考虑D-二聚体床旁检测。当需要快速报告结果时,床旁检测系统具有一定的优势。独立的POC分析仪可能需要与常规检测不同的质量控制,例如,有些系统提供电子的和液体的质量控制。厂家推荐的质量控制必须严格遵守。
可用的D-二聚体床旁检测一般使用全血、血浆进行检测。到目前为止,这些方法的临床性能研究相对较少。很多研究中,用于排除VTE的敏感度<97%,NPV接近或<97%,取决于方法本身和阈值。现在,没有一种床旁D-二聚体检测方法用于排除VTE已经通过了美国食品药品监督管理局的审批。
4.5其他技术
对于花费少效率高的自动化检测,在不影响灵敏度和特异度的情况下,检测样式应该尽可能减少冲洗和孵育步骤,使用最短的孵育时间。建立了很多固相和信号产生系统用于D-二聚体检测。此外,非均相检测、经典的定量微粒子凝集和进一步的均相技术也已经开展起来了。由于均相检测没有分离步骤,对自动化系统的要求是最低的。均相检测一般基于微粒子凝集的光散射原理,但是也有更复杂的信号产生系统如荧光能力转换测定(FETIs),荧光共振能力转移测定(FRET),和发光氧通道测定是主要适合D-二聚体检测的技术,可能在不久的将来可以生产出商业化的产品。
5.检测特性、参考区间和排除静脉栓塞的阈值
5.1推荐的检测特性
正确运用D-二聚体检测,特别是与PTP模型结合作为临床诊断流程的一部分,可以改进静脉栓塞可疑患者的评估效率。不正确的排除静脉栓塞,会增加患者的患病率甚至死亡率。用于排除静脉栓塞的D-二聚体检测必须满足一定的特性以保证患者安全。检测必须有高的阴性预测值、灵敏度,在阈值浓度水平有较好的重现性,以及有利于鉴别诊断的特异性。定量D-二聚体不能用于排除具有较高验前概率的患者。
用于排除中低验前概率静脉栓塞患者的D-二聚体检测阈值推荐的预测值特征见表3.在多数情况下,厂家提供了阴性预测值及其置信区间。推荐厂家不仅要提供检测的阴性预测值,还应该提供这方面的数据来源,例如同行评议问下或者监管或者认可机构的公共数据资源。检测的不精密度用变异系数CV表示。很多D-二聚体的检测报告的实验室内、批间CV不大于7.5%,这是定量D-二聚体检测应该达到的水平。厂家确定检测不精密度的指南见CLSI EP05。实验室验证精密度的指南见CLSI EP15.不同国家的要求不同。美国食品药品监督管理局FDA规定为0.98。
表3 用于排除中低验前概率静脉栓塞患者的D-二聚体检测阈值推荐的预测值特征

5.2参考区间
一项检测既有参考区间又有排除VTE阈值,可能会使临床医生感到迷惑。阈值可能与参考区间的上限相同,也可能不同。如果D-二聚体的检测的目的是排除VTE,则最好只要报告阈值,以免引起困惑,特别是当阈值和参考区间的上限不同的时候。这种情况下,参考区间也没有实际用处。很多实验室在进行检测时并不知道检测的目的,这种情况下推荐参考区间和阈值都报告。某些健康人群的D-二聚体会明显增高,例如孕妇、围产期妇女和高龄人群。D-二聚体检测排除VTE对于这些人群的诊断价值有限。当使用D-二聚体评估其他临床情况时,参考区间很重要,应该与结果一同报告,详见CLSI C28。
5.3 D-二聚体检测用于排除VTE的阈值建立:与临床表现和影像学研究比较
诊断DVT和PE的临床表现和影像学标准前面已有描述。阈值的建立需要对可疑的VTE患者进行D-二聚体检测,这些患者在检测前已经通过影像学技术进行了诊断。影像学诊断为阴性的患者,三个月之后需要重新进行评价以确认阴性诊断。根据以下程序进行预测值理论分析使“最终诊断”变成“事实”。此外,将临床诊断与D-二聚体检测结合仅局限于排除PE和近端DVT,不能用于评价其他部位的远端DVT和栓塞事件,包括UEDVT和主动脉栓塞。D-二聚体检测用于排除VTE的阈值设置是一个关键问题,检测结果低于这个阈值临床医生可以有把握排除VTE。因此,证明在阈值水平的检测性能能够满足检测前的标准是很重要的,这个标准保证了需要的性能和患者安全。
阈值确认研究需要大量病例,大多数临床实验室都不能收集到这么多病例。Steinberg等提供了阈值建立和确认研究的样本的量估计指南。样本量的大小取决于研究人群VTE的患病率、阴性预测值要求和检测的灵敏度和特异度。研究人群的患病率越高需要的样本量越大,因为假阴性数越多。如果排除了患者临床判断是PTP可能(高风险),只纳入了低风险的检测对象,则患病率小于10%,研究所需要的受试对象也相应的减少。但是,即使进行这样的验前筛查,还是需要数百例的受试者。此外,管理机构可能会要求分别建立排除DVT和PE的阈值,需要从多中心收集数据。
使用Steinberg提供的样本量估计方法,需要根据要求目标建立方法属性。但是,不管什么方法,阈值确认需要大量的样本。例如,检测方法的灵敏度为0.98、特异度为0.4,阴性预测值为0.98(95%置信区间的下限≥0.95)、功效为0.8、VTE的患病率为0.11,需要的样本大小为294(250例VTE和44例非VTE)。以上任何参数的改变都会使样本量发生改变。
最后,如果选择冰冻标本,则需要对冰冻标本和新鲜标本进行检测,证明这种方法检测此浓度水平的D-二聚体不会受到冰冻和冻融的影响。比较新鲜标本与冰冻标本的检测值。当新的检测方法与经临床确认过的检测方法进行比对,另一种方法是用常规检测的新鲜血浆标本与精密度研究(冰冻)标本同时检测,详见CLSI EP05。通过这种方法,适量的标本可作比较以检出检测方法间不常见的离群值。当比对方法和检测方法表现出高度相关,推荐使用这种方法。
5.4确定排除VTE阈值的方法
如果D-二聚体是用于排除VTE,实验室应该确定其阈值。确定阈值的方法有以下几种。
阈值可由厂家测定,并且由管理机构批准。此类信息可附带在试剂说明中,同样的方法均可用这个阈值。这是最好的方法。实验室应该意识到只有在排除PE或DVT时才能用这个阈值。以下方法是在厂家没有提供确认时采用,并应该谨慎使用。
阈值可以从同行评议文献中获得。实验室所用方法与文献中报道的方法相同。对研究要进行仔细评价,以确保样本量合适,统计功效足以确认得到的阈值。也可以通过其他实验室确定阈值,但是所得的值没有发表。这种情况下实验室必须知道数据的来源,并对数据进行总结来确定阈值,包括病例和非病例的例数、NPV值、灵敏度和特异度、统计功效。使用这种方法时实验室所用方法必须与研究所用方法相同。由于到达一定的统计学功效需要一定的样本,实验室可以用自己的数据来确定阈值存在一定的困难。各个地区不同,有些确定阈值的方法可能不被当地的监管和认可机构接受。推荐使用厂家提供的阈值。
有的实验室可能有多个地方进行D-二聚体检测。对于一些分析项目可在第二个检测处进行相关研究的确认检测,但是不推荐D-二聚体采用这种方法,因为不同地方所用的方法存在差异,可能会造成相关分析的误判。若两处使用的方法相同例外(仪器试剂盒试剂批号都相同);如果方法相同,但是试剂批号不同,产生的差异会更大,相关研究更困难或不恰当。
由于D-二聚体检测的复杂性,方法比对的分散性比一般单抗原自动免疫检测更大。此外,由于使用不同的抗体、技术,溶液处理方法不同以及试剂和稀释液的组成不同可能会显著影响其分散性。尽管有这些局限,不同的抗体和不同的检测技术得出了相对较好的相关系数。
5.5 令人满意的管理要求
厂家必须向监管机构提出新方法的批准申请,已通过申请的方法新增的功能也应该经过批准。并对其适用情况进行声明是“排除疾病”还是“辅助诊断”,见表4。
表4用于区分“辅助诊断VTE”和“排除VTE”的产品适应情况声明
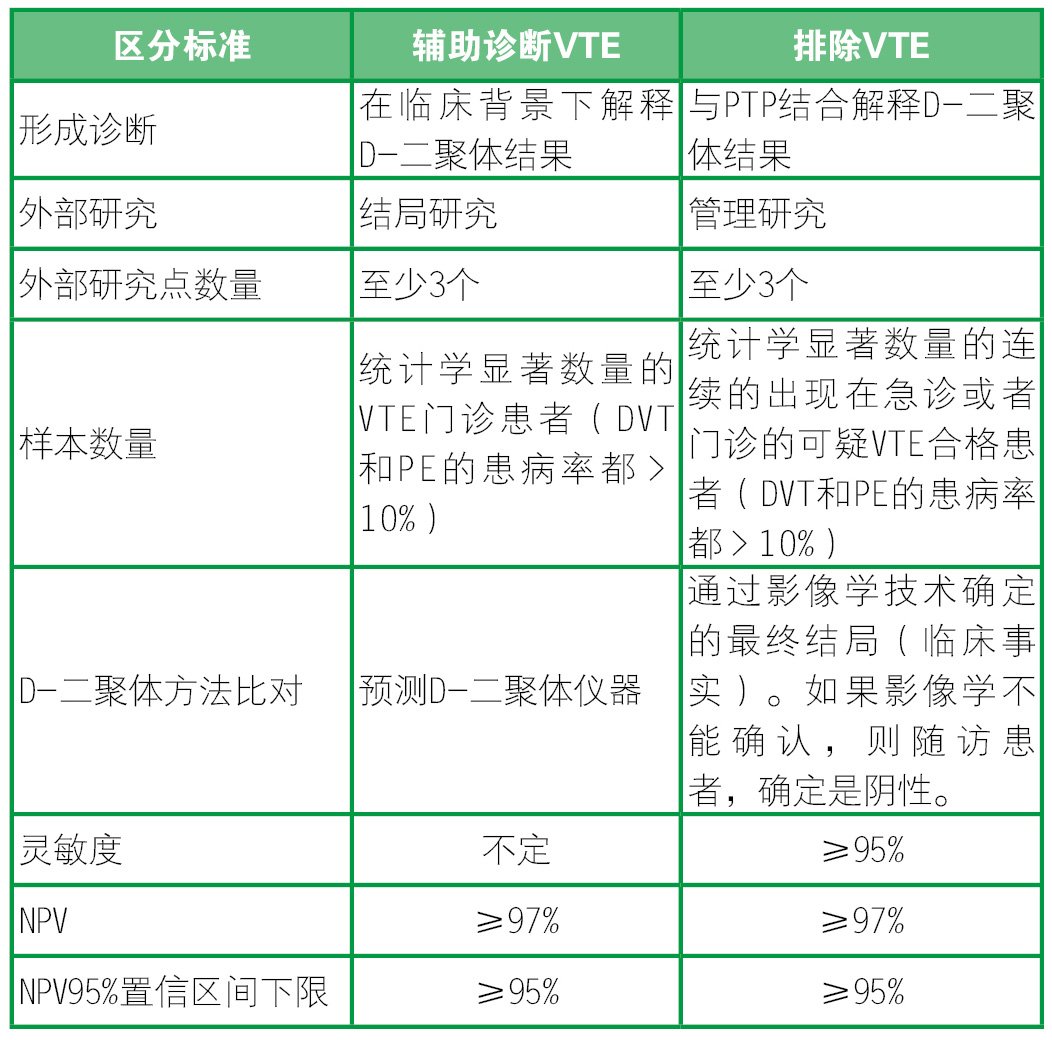
6 结果解释
D-二聚体是应用最为广泛的体外凝血活化标志物,主要是由于其在排除VTE中的作用。任何急性VTE可疑患者需要快速临床评估和客观的检测来进行准确诊断。
患者表现出VTE的临床症状(DVT的症状包括腿痛、劳累、肿胀、变色和水肿,PE的症状包括呼吸困难、咳嗽和肺相关的胸痛)应该首先用Wells或者修正后的Geneva得分进行评价。PTE得分是通过一些列危险因素和患者症状计算得到的。因此,PTP显示出无危险(或低中度危险)的患者应该考虑进行D-二聚体检测,PTP显示高危险的患者仅用D-二聚体检测是不能足以排除VTE的,还应该进行影像学检测。
患者的风险等级决定了即将进行的检测。例如,低风险的患者可做非侵入性的随访检测,高危险的患者应该进行更多的侵入性影像学检查。D-二聚体检测是一种非侵入性方法。随着PTP得分的增加,阳性D-二聚体检测结果为真阳性的概率会增加,因此阳性预测值(PPV)会增加。但是这尚未进过临床确认。当PTP得分降低,阴性D-二聚体检测的是真阴性的概率增加,NPV增加。
如果D-二聚体检测用作排除VTE的PTP已经在临床研究中得到了确认,则可减少进一步检测,节约检测花费。D-二聚体的结果解释与建立的方法阈值有关。一种方法阈值不能转换成另一种方法的阈值。阴性结果(低于阈值)且风险评分为中低度风险可排除VTE。阳性结果(高于阈值)预示了纤维蛋白降解产物异常,但是不是VTE特异性的,需要进一步评价,见图1。
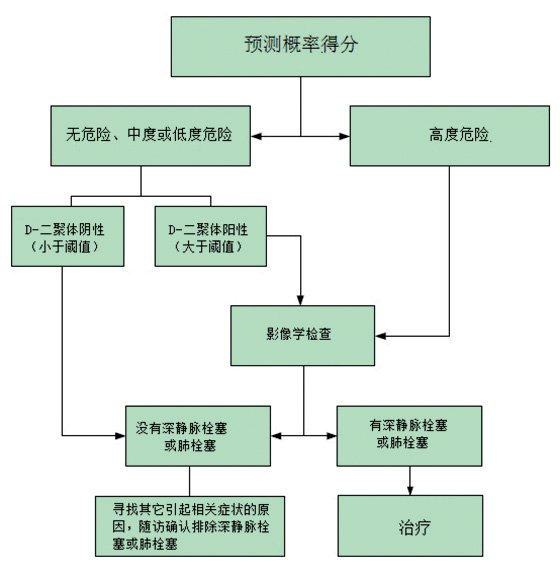
图1 深静脉栓塞或者肺栓塞的诊断流程
6.1 结果报告
有的厂家基于存在的D-二聚体片段的量,以DDUs报告D-二聚体的浓度。有的采用FEUs报告。结果报告的形式和单位按照厂家推荐,不要对单位做任何转换。单位FEU是假设一个纤维蛋白原分子产生两个D-二聚体片段,通过产生D-二聚体片段的纤维蛋白原的量来表示FDPs的。FEU等于D-二聚体片段的量与纤维蛋白原分子的比值,因此,FEU表示的D-二聚体的量是DDU表示的1.7倍。在临床上常用2作为转换因子。正如下文强调的,这些数学转换是不可接受的。更为复杂的是厂家可能用不同的单位表示例如:纳克每毫升、微克每升、微克每毫升或毫克每升。尽管有几个厂家使用500 μg/L FEU排除DVT,但是最近的meta分析报告了很宽的阈值范围。临床医生误认为所有的D-二聚体检测的阈值都是500 μg/L FEU。实验室应该报告所用单位及其排除VTE的阈值。厂家应该在每种方法所用试剂产品上标识报告单位和阈值 。不同单位间的数学转换是不可接受的,因为会增加报告中的错误。
图1展示了使用PTP、D-二聚体和影像学检查诊断VTE的流程。也提出了其他相似的方法。Michiels等将临床、实验室和影像检查相结合对DVT诊断方法进行了修订,减少了重复进行超声检查。使用这些标准化的方法可减少侵入性检查,降低诊断成本,提高诊断效率。