基于电化学检测的DNA微阵列
——为临床诊断和药物检测开发多元化基因型检测系统
Robin H. Liu, William A. Coty, Michael Reed, and Gary Gust
编译:王佳芳
到目前为止,多元化技术例如实时聚合酶链式反应(PCR),在一次检测中只能分析数目较少的多态现象。DNA微阵列多路技术能力的开发,增加了可以同时确定独立基因型的数目。早期的微阵列重点在高密度设备,这样很适合用于发现基因。现在新的探测技术和简化方法的发展更加有利于把昂贵的高密度阵列转换为划算的,由低到中等密度系统,应用于临床诊断和药物检测设备中。
绝大部分的微阵列方法使用了光学探测,例如荧光法,发光法,或者随后固定在表面固定传感器上的金纳米粒子标记探针。在一些情况下,多色标记方法允许应用于多元化识别中。例如,Nanosphere Inc. (Northbrook, 伊利诺斯州)公司的Verigene系统,使用基于金纳米粒子的微阵列平台分析了单一核苷酸的变异。AutoGenomics Inc.(Carlsbad, 加利福尼亚州)开发的Infiniti BioFilmChip,在基于薄膜的微阵列上利用荧光探测进行基因组和蛋白质组的分析。一般来讲,基于光学的探测需要大型的昂贵的扫描仪,或者基于电荷耦合器件的成像系统。
开发一个划算的设备和小型的床旁检测DNA诊断系统,IVD公司已经采用了多种不同的方法进行DNA杂交的电子检测。这种系统的微阵列可以由便宜的硅化物,陶瓷物或者基于印刷电路板的制造技术进行生产。
电化学检测方法可以应用在临床化学,特别是用于糖尿病护理的血糖监测,然而,虽然大量的研究表示分子诊断技术基于电化学探测,到目前为止却没有达到有效的应用。
Osmetech Molecular Diagnostics (Pasadena,加利福尼亚州)的eSensor囊性纤维化载波探测系统是一种基于电化学探测DNA的微阵列产品。已获得美国食品及药物管理局的认证并应用于临床。这个系统包括eSensor 4800设备,以及23个突变基因型和囊性纤维化跨膜调解基因的一个多态性基因型检测的试剂及试剂盒。这个方法被美国产科及妇科医生学会以及美国医学遗传科学院推荐为载体筛选。

图1:Osmetech诊断的eSensor XT-8系统(帕萨迪纳,加州)
本文论述了一个新的eSensor系统,包括了eSensor XT-8设备,微流样品管(见图1),这个系统的新特点包括增加阵列密度,减少杂交时间,以及更加简洁和标准的设备设计,提供了真实的随机存取操作和用户友好的触摸屏监视器,模块的设计使设备的容量和产量可以进行变化,来满足小型医院实验室到大型检验所的检测需要。eSensor XT-8系统开发的第一个临床设备是eSensor杀鼠灵灵敏性检测,为进行美国食品及药物管理局申请在国内及临床中对性能进行评估。然而,工作特性还没有完全确定。
DNA检测技术
eSensor微阵列由一个印刷电路板(PCB)组成的,这个电路板由一列金制的电极组成。每个电极由一个多成分的自组装单层膜进行修正,单层膜包含寡聚核苷酸合成前的捕获探针(见图2)。核酸检测是基于夹心化验原理。信号和捕获探针的设计为与序列互补,在相应靶DNA序列的临近区域。基于序列特异杂交原理,一个三元复合物会在捕获探针、靶标以及信号探针之间形成。这个过程使含有电化学活性二茂铁标记的信号探针的5''''-末端非常接近于电极的表面。
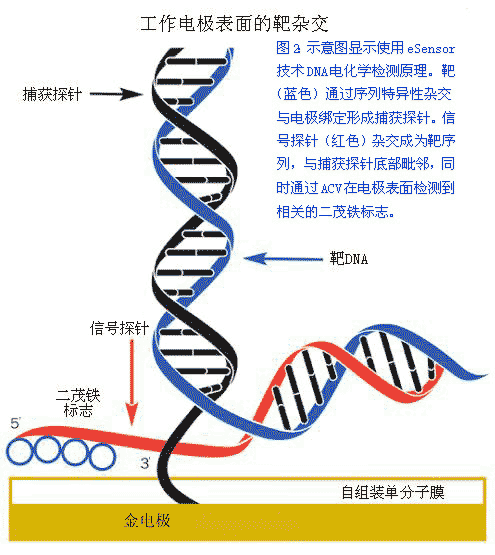
每个二茂铁组的亚铁离子进行循环的氧化和还原,导致电子得失,这可以在电极表面使用交流电伏安法(ACV)以电流的形式测量出来。高度有序的谐波信号分析也可以辨别基于二茂铁来自于后台电容反馈的感应电流,使用这种方法,eSensor技术的探测灵敏性可以测量大约10pM。当与PCR扩增相结合的时候,电流灵敏度足够进行基因型检测的应用。其他的方法已经证明电化学检测的灵敏度增加。
使用ACV进行电化学检测,谐波信号分析,自组装单层膜的结合,高度抵制了来自样本成分的干扰。使用荧光检测时正常情况下会造成干扰的血液成分(例如:血色素,胆红素),使用eSensor技术时不会对信号检测造成影响。另外,二茂铁标记的氧化和电流通过单层膜的传递取决于标记和单层膜表面的接近程度。结果,没有检测到游离的信号探针,在ACV检测之前不需要清洗过程去处游离试剂,甚至当代表多个靶序列的大量信号探针出现。化验过程是简化的,允许杂交和检测在没有流体处理或废物盒的小印记设备上进行。相反,常规的微阵列需要机械设备自动操作多级流体处理过程。这些设备体积大,结构复杂,并且昂贵,价格高但微阵列的应用有限。
基因型化验原理
突变或者杂交的基因型检测使用二茂铁标记的特定等位基因信号探针来进行,二茂铁携带了可辨别氧还电位。与野生型序列相匹配的信号探针包含一种电化学电位的二茂铁标记,与突变序列匹配的信号探针包括另一种可辨别的二茂铁标记(见图3)。野生型和突变型靶标都连接到位于突变邻近位点的捕获探针上,野生型和突变信号探针会竞相结合到它们的互补序列。
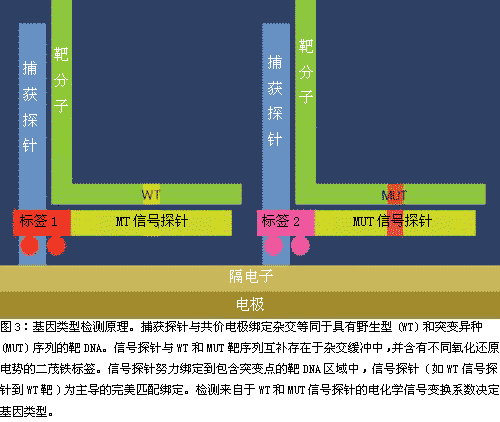
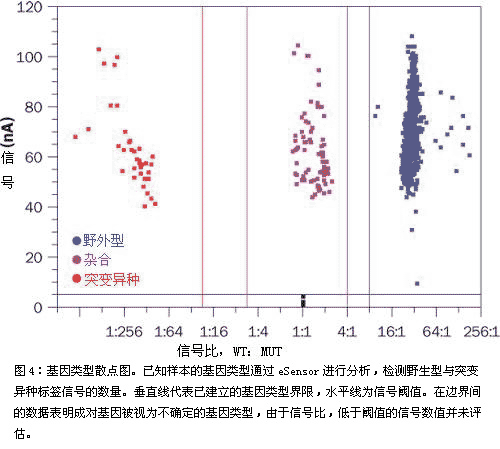
与靶标相匹配的探针会得到优先选择。基因型由结合的野生型和突变型信号探针产生的信号比率来确定(见图4)。基因型的分界线是基于大量样本数据的统计学分析建立的。未知样本的序列识别不需要进行对设备或者试剂批号进行进一步校准。这种方法可以区分单一或者多重基础的改变,插入或者缺失。一个含有多重等位基因突变位点或者两个邻近的突变位点都可以使用附加的二茂铁标记来确定其基因型。
系统概述
eSensor XT-8多通道基因芯片分析仪包含了一个PCB芯片,一个盖片,和一个微流组件(见图5),PCB芯片包括72个金制板工作电极(与用于囊性纤维化载波检测芯片的36个电极相比较),一个银/氯化银参考电极,两个金制板辅助电极。每个工作电极有接口与芯片反面的垫片连接,以便与eSensor XT-8设备进行电连接。(见图5d)。
多通道基因芯片分析仪也包括一个电可擦除可编程只读存储器组件,存储试剂盒信息的内存设备(例如:化验标示符,试剂盒批号,有效期)。微流组件包括一个平板和一个层压板,层压板包括膜片泵和止回阀,造成曲折的通道以便于形成电极列上方的杂交室。
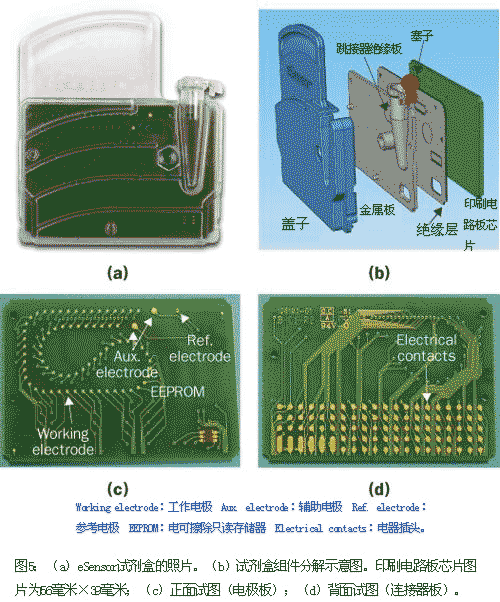
进行eSensor化验的准备时,PCB芯片会使DNA捕获探针和工作电极上的绝缘分子沉淀。每一种特定的沉淀溶液使用自动吸液管系统分发给适当的电极。捕获探针和绝缘器与金制表面反应产生绝缘的自组装单层膜。15 捕获探针分发完之后,PCB芯片洗涤,干燥并且与层压板、平板、塑料盖片装配成一个盒,形成一个微流循环系统,可以保存大约140μl.
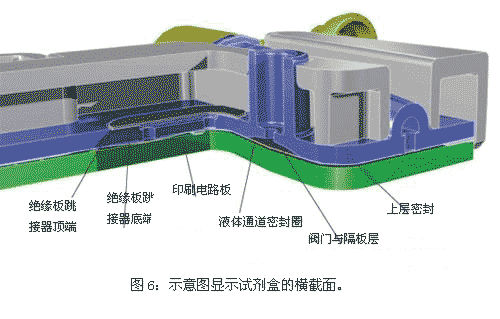
多通道基因芯片分析仪内的膜片泵与eSensor XT-8设备的气流源连接,在杂交过程中通过微流通道为杂交混合物提供单向的充气(见图6)。使用微流技术使杂交溶液在电极表面流通,使未搅动界面层最小化,并能不断的补充电极上方耗尽的互补靶标序列以及信号探针。16这个过程使杂交时间从使用囊性纤维化载波探测的2小时缩短到30分钟甚至更短。
eSensor XT-8设备有一个模块设计。包括了基本模块和分别包含了8、16或者24槽的1个、2个或者3个处理塔(见图1和7)。塔的数目根据产量需要有所不同,并且当实验室产量需要增加的时候,设备可以加固安装新的塔。假如需要30分钟用于杂交和检测,三塔系统的产量就可以达到每8小时300次检测。

在典型的临床试验室里小印记系统(一塔系统46 × 40 × 41cm三塔系统46 × 65 × 41cm)保存了台空间。盒槽之间互相独立操作。每一个数字的盒都可以同时装载,剩余的格在设备运行的时候仍然可以使用。当一次检测完成之后,那个格就可以应用于另一个盒上。
基础模块控制每个处理塔,提供电力,存储和分析数据。基础模块包括用户界面,和一个15-英寸的人像定向显示器和触摸面板。设备的设计为使用触摸屏界面进行单独操作。键入患者编号和试剂批号编码可以使用条形码扫描器,触摸屏,或者u盘上载文本文档来进行。
处理塔包括8个模块格,每个格包含盒接口,精确控制加热器,抽气机,和电子元件。盒接口的设计可以达到高度的可靠性以及很长的寿命。抽气机驱动盒内膜片泵和阀系统,消除设备与盒之间的液体接触,使盒的复杂性和成本降至最低。
临床应用
杀鼠灵是美国最常用的处方抗凝血剂,17然而,它的治疗学范围很窄,广阔的个体剂量差异需要达到最佳的治疗效果,药物过量会出现严重副作用,主要是过量出血。18 Osmetech开发的eSensor 杀鼠灵灵敏度检测是eSensor XT-8系统的第一台设备,检测可以确定与杀鼠灵剂量相关的两个基因的三个多型性,并允许基于基因型的个性治疗。
在肝细胞色素P450(CYP450)2C9作用下,更多活化的杀鼠灵S-对映体,产生代谢变化成为不活跃形式。基因CYP450的两个多型2C9(*2, *3)还原了酶的活性,并且杀鼠灵剂量的减少与副作用的增加是相关的。
维生素k环氧还原酶(VKOR)参与了反应路径,并且导致了凝结因子的活化,成为杀鼠灵反应的靶标。一个杀鼠灵灵敏单模标本被识别,然后多型-1639G>A启动子可以识别带有杀鼠灵灵敏基因型(-1639AA)21的患者。
杀鼠灵灵敏度化验包包括一个PCR缓冲器——内含引物以及dNTPs,耐热的DNA聚合酶,核酸外切酶,以及基因型检测试剂——包括信号探针,盒和附属缓冲器成分。检测开始时,添加PCR母料,与基因组DNA样本混合,混合物将会在标准设备中进行热循环。PCR之后,所有的产物用抗菌素Ⅰ核酸外切酶进行简单处理,这种外切酶可以特异识别和处理不属于预定靶标的扩增子。
不需进一步净化的条件下,PCR全部的产物以及核酸外切酶的消化物可以用于检测基因型。基因型的检测需要添加试剂至消化后的PCR产物,试剂中包括特定的等位基因,二茂铁标记的信号探针。然后将混合物放在盒的样本库上。整个杀鼠灵灵敏度检测程序开始于单独的DNA,可以在4小时内完成。化验可以在eSensor XT-8设备的随机存取模式下进行,因为此模式对这项应用有益。
化验性能
在eSensor XT-8设备上进行的杀鼠灵灵敏度检测的性能已经从精确性,再现性,化验范围,和干扰物影响等方面进行了评估。检测40份相同的基因组DNA样本,在10,100和1000ngDNA/PCR上均给出100%的报告率,显示了宽泛的样本输入容许量,在大多数的商业全血gDNA提取试剂包里,这样的范围足以跨越预期DNA产量的上限和下限。
精确性评估是使用eSensor方法和与双向DNA测序技术来比较101基因组DNA样本基因型测定。一致性为100%,97%的样本在第一轮检测后给出了结果,在无报告结果重检之后,报告率为100%。再现性通过检测一组20基因组样本和3个质粒控制来进行评估,这些质粒控制象征了所有可能基因型组。组的检测用3个批号的杀鼠灵灵敏度检测包在5个单独日里进行。这个协议使用3个设备进行总数为345次的检测。eSensor结果与DNA测序的一致性为100%,100%的样本在第一轮检测之后给出了结果。
评估杀鼠灵检测中潜在干扰物质的影响时,向全血中添加下列物质:人血清白蛋白(3 g/dl),人类IgG (3 g/dl),胆红素(0.3 mg/ml), 甘油三酯(500 mg/dl), 血色素 (20 g/dl),以及乙二胺四乙酸(浓度大于4倍抗凝浓度,用于模拟少量血流)。试验之后,抽取基因组DNA,检测基因型。这些物质都没有影响PCR的效率,基因型的报告率或者精确性。
产品菜单
产品的开发最近重点在遗传药理学和遗传病的化验。Osmetech正在开发eSensor杀鼠灵灵敏度检测组的外延,可以用于确定基因CYP450 2C9的8寡聚核苷酸多态性(SNPs)基因型。这些基因型和VKOR-1639G>A以及基因CYP450 4F2(rs2108622)134G>A 19的多型会降低酶的活性。CYP450 4F2 SNP的基因型22,大约占到了杀鼠灵剂量个体差异的15%。
等待美国食品及药物管理局审批的这项检测可以识别患者杀鼠灵副作用增高的风险,有助于使用公布的运算法则来确定早期最佳的杀鼠灵剂量。2C9 SNPs也可以识别患者由于CYP450 2C9酶引起其他药物代谢产生的药物过量风险。例如:苯妥英(一种抗癫痫药),格列吡嗪和甲糖宁(抗糖尿病药),塞来昔布(非类固醇的抗炎药),氯沙坦(一种血管紧张素Ⅰ受体阻断剂)。
其他处在发展阶段的检测包括附加的细胞色素P450标记物基因型检测——与一般药物代谢相关,传染病检测,与特定药物治疗的代谢和功效相关标志物的化合物检测。
美国食品及药物管理局最近鼓励遗传药理学生物标记物的鉴定和确认的成就是从遗传学,癌症,传染病和遗传药理学上获得了新的诊断机会。24这些新的标志物可以适用于临床试验室的平台和提交美国食品及药物管理局认证。这样会提供容易使用的,划算的检测,应用于所有规模的医院里。
总结
电化学探测允许电子元件进一步小型化和上游样本抽取和扩增过程的整合,前期的研究显示了一次性,结果装置eSensor设备的可行性,最近微流的发展提供了额外的工具执行所需的功能。25,26使用核酸的电化学检测开发一种床边诊断微阵列系统,可以满足临界卫生保健需要,包括在医院和床边装置的心脏护理单元和传染病检测中,快速检测基因型以便辅助确定精确的杀鼠灵剂量。
参考书:
1. M Huber et al., “Automated, Enzyme-Free Genotyping Directly from Human DNA,” IVD Technology 13, no. 6 (2007): 37–45.
2. R Vairavan, “An Automated Multiplexing Platform for Genomic and Proteomic Analyses,” IVD Technology 14, no. 1 (2008): 29–35.
3. KL Gunderson, S Kruglyak, and MS Graige, “Decoding Randomly Ordered DNA Arrays,” Genome Research 14 (2004): 870–877.
4. J de Leon, “AmpliChip CYP450 Test: Personalized Medicine Has Arrived in Psychi?atry,” Expert Review of Molecular Diagnostics 6, no. 3 (2006): 277–286.
5. M Schena, Microarray Biochip Technology (Natick, MA: Eaton Publishing, 2000).
6. P Fortina et al., “Simple Two-Color Array-Based Approach for Mutation Detection,” European Journal of Human Genetics 8 (2000): 884–894.
7. J Wang, “From DNA Biosensors to Gene Chips,” Nucleic Acids Research 28 (2000): 3011–3016.
8. ND Popovich, “Mediated Electrochemical Detection of Nucleic Acids for Drug Discovery and Clinical Diagnostics,” IVD Technology 7, no. 3 (2001): 36–42.
9. KM Roth et al., “Electrochemical Detection of Short DNA Oligomer Hybridization Using the CombiMatrix ElectraSense Microarray Reader,” Electroanalysis 18 (2006): 1982–1988.
10. K Kerman, M Kobayashi, and E Tamiya, “Recent Trends in Electrochemical DNA Biosensor Technology,” Measurement Science & Technology 15 (2004): R1–R11.
11. M Reed and W Coty, “eSensor: A Microarray Technology Based on Electrochemical De?tection of Nucleic Acids and Its Application to Cystic Fibrosis Carrier Screening,” in Microarrays: New Development Towards Recognition of Nucleic Acid and Protein Signatures, ed. K Dill, R Liu, and P Grodzinski (New York: Springer, 2008).
12. MS Watson et al., “Cystic Fibrosis Population Carrier Screening: 2004 Revision of American College of Medical Genetics Mutation Panel,” Genetics in Medicine 6 (2004): 387–391.
13. TM Nahir and EFJ Bowden, “The Distribution of Standard Rate Constants for Electron Transfer between Thiol-Modified Gold Electrodes and Adsorbed Cytochrome C,” Journal of Electroanalytical Chemistry 410 (1996): 9–13.
摘自IVD Technology 2008年第五期
版权归原作者所有,仅供内部学习