注册登录才能更好的浏览或提问。
您需要 登录 才可以下载或查看,没有账号?立即注册
×
James K.Tusa 于1980年获得芝加哥大学理化博士学位,于1988年获得洛杉矶加利福尼亚大学工商管理硕士学位。他曾任Osmetech公司副总裁,在前AVL公司工作长达10年 ,现任高级顾问。在此之前,他曾在位于美国明尼苏达州首府圣保罗的3M公司总部任职项目经理。以及在两家刚起步的涉及医疗器械和诊断的公司:CDI和Gen-Probe任职系统管理员。他的研究方向是荧光和光谱学。
Huarui He 于1983年获得中国天津南开大学化学分析学理学学士学位。1992年,于奥地利取得格拉茨大学有机化学博士学位。毕业后,被AVL公司聘为首席药剂师。AVL公司在2000年被罗氏诊断公司收购,之后于2003年由Osmetech 公司收购。他的研究方向是荧光探测器和光纤生化感应器的综合体。
本文总结了在测量全血危重护理分析物时,荧光传感器在体外诊断系统中的应用。我们探讨了在该领域使用荧光指示剂的荧光化学传感技术近来取得的进步。本文涉及到了主要材料、构效关系、以及低成本在便携系统中实现高效用的设计理念。在该应用范围内,与当前传统的电化学传感技术相比,光学传感技术突显了与其相当甚至更好的精确性和稳定性。
介绍
光学传感器中,光介质的改变即是传导过程,这一概念已被人们熟知数十年了。20世纪60年代,人们发明了这种使用光纤的传感器并将其用于血氧的测量中。20年后这种传感器出现在了葡萄糖比色条和荧光血气监测的电极上。而且,由于近年来通讯工业和光学开关部件,以及高质量的光纤和光学波导技术的发展,促进了光学传感器或者说“荧光电极”的快速发展。
光学传感最初仅限于有内在吸光度或荧光度的物质中,但随着某些关键指示剂化合物和耦合器连接到接收器中的发现,使得该技术延伸到许多参数的测量中;例如血气(氧气,二氧化碳,和PH);近期更是延伸到了电解质和代谢物;例如葡萄糖,乳酸盐,尿素和肌酸酐。在许多情况下,使用荧光进行测量;这也是本文重点讲解的内容。荧光过程如图1所示。特定化合物可能会被刺激到一个具有较高电子能量的水平,当再回到基态时,它们会释放出光子,这个过程被叫做发光。但是当光用于提供激发能量(而不是用于化学或者电学)时,它被叫做荧光。其它形式的发光包括化学发光,生物发光,电化学发光和磷光等。

图1光激发染色分子而释放光和荧光
合适的分子设计和对分子环境的控制,发光过程可能由于某血液分析物的存在而被调整。例如,当氧存在,某些有长时间激发态的指示剂分子,其荧光性会根据样品中氧气含量的多少而停止或减少。因而提供了一种检测的方法(见图2)。
这种情况下,通过放置使用期长的荧光团到高氧浓度的分子环境中,即使很低的氧分压也会改变传感器而被测量,比如:聚二甲硅氧烷。对于PH的测定,一个荧光PH指示剂染色固定于某一种亲水的铸模中,例如改良的聚氨酯——染料与氢离子可逆结合,荧光强度的变化与pH成比例。对于二氧化碳的测定,该系统放置于一透气薄膜后,通过该薄膜,二氧化碳扩散,并会引起此处PH值的降低。
荧光电极区别于电极的一个主要特征是它不需要参比电极,给可靠、经济的一次性应用提供了稳定操作和廉价制造的优势。而且,荧光极不消耗直接测量的任何分析物的分子,例如,氧分子。(间接光纤生物传感器除外,例如:外加生化酶的光学传感器,其可以测量酶反应物的浓度变化,比如氧气,或例如过氧化氢的反应物)。因此,没有参比电极,以及可逆的非消耗性操作,相对于电化学传感器而言,一般认为荧光极在血液中更加稳定,这一点可以通过它们在连续或接近连续的血气监测中,极少出现重新定标的性能得以证实。荧光电极有两个弱点:他们通常需要比电化学更加复杂和昂贵的测量仪器;为了良好生产和操作的需要,要求高额的研发经费用于合成和固定染色系统。
荧光电极中两个主要的构型已经发展到医用领域。第一种类型将生物传感器放置在一个光纤的顶部,这种类型已用于体内诊断,例如:将其在人体的桡动脉内滞留几日进行血气的系统监测。对于体外诊断应用包括在此描述的 OPTI 系统,化学传感器放置在一个平直的光学透明支座上,并称为平面荧光电极。
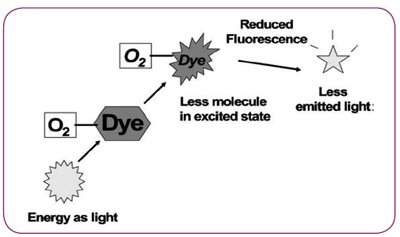
图2 由于氧与染料分子结合导致的荧光减弱
临床应用的基本要求和物理特性
分析迅速变化的血液分析物,并对充分评估、稳定和管理危重病人是非常重要的。鉴于明显稳定的病人大量血气和其它快速改变的分析物亦会发生自然变异,有人曾经主张应连续、在线检测趋势的基础上做出临床决定。然而,在过去的几十年里,虽然技术上取得了极大的突破,但是真正连续的血管内测量对危重病人是不够可靠和经济的。这样就给下一个最好的临床选择的增长提供了发展空间,在床边进行的‘POC’测量缩短了治疗决定的时间, 被定义为发出血液测量指令和获得其结果之间的时间。 另外这些系统必须提供实验室质量的结果,无须将维护和可靠性方面的问题添加到繁忙的危重护理科室的日常活动当中使其复杂化。
所谓的“危重护理”分析物包括血气(O2、CO2、pH),电解质(Na+、K+、Ca2+、Cl-),和特定代谢物(葡萄糖、乳酸盐、尿素、肌酸酐)。传统方法上,这些分析物是在大型的台式分析仪上进行分析,内置多种定标液体需要时常的对电极重复定标。测量血气和电解质的传感器电极是微型电极,其专门用来测量相对于参比电极的电位差(除使用‘Clark’电极对PO2进行的电流测量之外);代谢物的测量使用所谓的采用了生化酶的生物传感器,通常将其固定到一个能够测量酶生成物或反应物的电极上,例如:过氧化氢。在病人床旁进行POC测试的强烈需求持续地推动了便携式系统的发展,便携式系统利用小型一次性传感器可快速精确地进行全血测量。 因为分析仪的核心就是传感器,那么企业必须改良传感器技术,以满足小体积、高稳定性、经济、可靠以及免维修的新要求。所以,实用且便宜的传感器发展以及在全血中这些分析物的临床诊断系统占据了重要的研究领域。
识别和转换的一般传感原理
传感器可以被认为是这样一种设备,这种设备没有试剂,且与化学或生物分析物相互作用,并以信号反应一种可测量的变化。迄今为止,许多科学家和临床医生认为传感器如pH电极一样,是一种宏观仪器,可以用来测定危重血液分析物像血气,电解质和代谢物。然而伴随
着纳米技术和主客体分子识别技术的进步,没有理由不考虑将适合设计的个体分子作为传感器。在微观上,大多数传感器包含一个感受器或一个识别元件(可以在一定生理浓度上对化学结合或分析物的辨别有足够的选择性),以及帮助将这种结合过程转化成可测量信号变化的转化元件,可能是光学的,电化学的或其它(见图3)。
在宏观层面,许多危重血液分析物传感器依据转换因子的不同可以分为电化学和光学两类。相应指的是电极或者荧光电极。有些时候,他们使用识别步骤而非元件;比如Clark PO2电极并没有识别元件,而是直接通过氧气的减少量测电流。
识别元件或者“接收器”由于他们的结合强度和可逆性而不同。许多接收器,像钾离子颉氨霉素和氯化离子转换物,两者都常用于离子选择性电极(ISEs)中。相对微弱和可逆地与它们的目标分析物结合。其它识别元件如抗体定位低浓度心肌标志物,以及来自传染性物质的DNA探针目标追踪核酸低聚物,通常强烈且不可逆地与目标分析物结合;若用在可重复使用的结构中,它们必须进行特别的包装、再生以释放它们的目标。分子识别化学家利用术语“化学传感器”来形容使用无生命、人造识别元件的传感器,利用“生物传感器” 来形容使用有生命的、来源于自然的识别元件:如生化酶传感器。使用生化酶的生物传感器通常有选择性的结合分析物,并且催化其转换成一个不同的分子,使其可以被传统的化学传感器检测到。例如氧化酶:葡萄糖氧化酶,在氧化目标分析物的同时消耗氧气并产生过氧化氢。使用酶的生物传感器通常比化学传感器有更好的选择性,然而相对于化学传感器系统而言,一些常测量乳酸和肌氨酸酐的酶系统,当储存在湿的地方或分析仪中时,其稳定性较差且迅速失去活性。
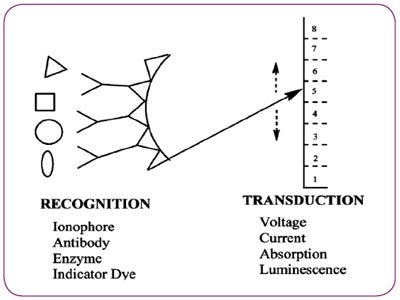
图3 传感器识别和转换元件
传感器有时被固定在膜基质中,通过降低渗出到疏水部分的血液以延长其重复利用和使用期限。
一个传感器不仅需要一个接收器,不经过一些转换系统,目标也许会受限,但不会被检测出。转换元件或过程可以确定已发生的化学结合的数量或比率,例如:传感器原料的电或光学属性的改变。危重护理分析物的电化学传感器尤为强大,依靠电极电位与一个参比电极对比测量分析物,或者由安培计测量一个由电化学反应产生的电流。样本转换系统包括电位离子选择性电极,可测量被离子载体分子束缚的离子在传感器表面产生的电位。葡萄糖电极,可测量由生化酶转换成葡萄糖导致过氧化氢氧化而产生的电流。氧电极,当氧分子在染料分子周围分散并引进非辐射的转换时,测量到荧光减弱或停止。酶转换成葡萄糖产生过氧化氢,使用比色葡萄糖测试条,可检测到燃料分子颜色的变化。总之,转换系统决定了传感系统的“获得”。也就是测量输出的扩大与识别步骤的数据或比率有关,在下面将会介绍。
传感系统有四项“S特点”也就是,敏感度,选择性,速度性和稳定性。敏感度或响应度是识别元件结合常数的函数,是结合过程中转换元件的转换和扩大(信号)对比外来无关过程(噪音)的函数。尽管传感器必须在分析物浓度的整个病理范围内显示回应, 但分析物浓度中单位百分比变化的响应度或“斜率”,确定为病理浓度时,对于非溯源的分析仪而言,比起“最小可测量数量”是一种更为有用的性能系数。传感器的选择性是衡量其对预期分析物相对于其它分析物或基质内的干扰物种的敏感度,通常将其表示为一个没有单位的对数比例值。选择性通常仅是识别元件的功能,且经常受到一种干扰分析物的影响。例如钾离子载体对钾变化的敏感度至少是对钠变化敏感度的300倍,否则,Na离子±30mmol L-1的变化(中心近140mmol L-1)将会导致明显的钾离子大于±0.1mmol L-1 (中心近4.5mmol L-1)的变化,这将会引起临床上非常巨大的变化。在某些情况下,传感器在有其他可测量的干扰物时,不具备足够准确的选择性,只是数字上对该特定干扰物进行更正。例如:为测量的钠更正锂传感器,为测量的离子钙更正镁传感器。传感器的回应速度是在回应时间与阶跃函数的0-95%之间,回应函数通常是指数函数的一次方或二次方。传感器的速度通常由传感器薄膜的厚度决定,由于在传感器薄膜内的扩散过程,通常与传感器的稳定性相平衡。然而,通过使用端点检测或预先计算法则,表现速率得以提高,但是这是以牺牲精确度为代价的。最终传感器的稳定性指的是传感器主要定标指数的稳定性,比如在测量分析物缺失情况下的荧光强度比率。传感器回应函数的稳定性对于定标的类型和频率是一个重要的决定因素。使用电极的传统台式分析仪频繁执行1点定标来纠正它们的基线(例如,应对蛋白质沉积),偶尔执行2点定标以纠正敏感度或斜率的下降。用在OPTI 上的一次性光学传感器仅执行一次1点定标,因为它们的斜率非常稳定,每批定标值通过条形码输入仪器。由于敏感度和背景信号的稳定性,一次性干燥存储的物品如某些葡萄糖试纸无需定标。
科学家们之间常常就一个问题展开辩论:光学或电化学传感器技术哪个更好?答案是:“传感器技术的好坏取决于它的应用、构造以及执行的灵敏度”。由于在光学发射管标准化输出,在背景反射和荧光不可控制变化中维持光学定标都存在着困难,所以光学数量转换系统通常比电气化学要求更为复杂和昂贵的测试设备。然而,由于蛋白质沉积在参比电极上,导致电器插头和参比电极通常不稳定,所以电化学传感器的制造比光学传感器更为复杂和昂贵。一般来说,因为电化学传感器本质上依赖表面现象,所以它比光学传感器有更快的反应,例如,电极表面的自限充电积累,但是光学传感器通常可以依靠传感器层面的大量扩散而更加敏感。
两种类型都存在着干扰问题——光学传感器一般要求使用薄膜来筛选血浆中有颜色的材料,如胆红素和自由的亚铁血红素,但是电化学传感器对于电活性干扰物非常敏感,如:抗坏血酸盐和对乙酰氨基酚。一般而言,光学传感方法如吸光率、发光法以及荧光技术在大型的临床化学和免疫测定分析仪上占据了主导地位,然而电化学传感器更加立足与全血/血清重症分析物的测量,如:血气、电解质以及代谢物。新一代的床旁分析仪出现了两种类型的小型传感器,但是目前还不清楚哪个会占据主导地位。表1总结了重症监护分析物以及它们要求的测量范围、敏感度和选择性2。
以上提到的这些“S特征”对于医疗用户来判定主要系统特征如:精确度、准确性以及周期方面起到了极大的作用。比如:精确度很大程度上取决于敏感度和定标稳定性,典型地表示为日常的1SD或1RSD测量20天内稳定的安瓿液体材料,这一点在NCCLS3c指导方针中有详细的阐述。典型的竞争条件是1-3% (pH±0.02),且在表1中有描述。全血、血清或血浆中的准确性既要求精确度也要求选择性,也就是说,由于血液复杂基质内的较大和较小的干扰物而没有偏差,这种情况在病人之间是非常不同的。为了评估准确性,新的系统必须与一个参照的分析仪(使用从医院内成千上百个病人身上获取的血液样本)进行并行比较。最好是使用不同的参照分析仪在多家医院对血清、血浆或全血进行重复测量,然后使用线性回归配对结果,由此得到了斜率和偏差在数量上的评估。通常预计回归斜率必须降低10%以内,平均偏差(接近中等病理分析物水平)应当下降到5%以下。周期是测量中最短的时间,通常由传感器响应时间(与敏感度和稳定性有关)来决定,定标频率也由传感器稳定性来决定。一般情况下,重症监护系统每小时最少可进行15个全血测量,有的能够执行30-40个测试。
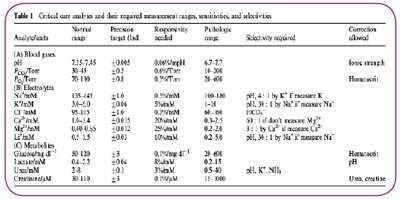
表1 重症分析物及其要求的测量范围以及灵敏度、选择性
诊断应用的荧光技术以及其原料要求
在医院环境下,首次使用光学测量的重症监护分析物是血气,当时采用的是19831b年引进的CDI “Gas-Stat”系统。该系统的性能足以进行持续的“趋势检测”,然而首次引进时,许多临床专家认为该系统不够精确和稳定来替换周期的体外测量。它的传感器采用了与随后的荧光电极系统相同的原理。9年以后,即1994年,位于奥地利格拉茨和美国乔治亚州罗斯威尔的AVL Scientific Corporation研发了便携式体外诊断测试OPTI 生产线。该系统包含了一次性和可重复使用的测试片(下面将会详细描述)以及一台可测量光学荧光和反射的小型、便携内置微处理器的仪器(见图4)。OPTI系统可测量全血中的8种分析物,使用120微升全血在2分钟内执行测量。该系统被罗氏诊断于2000年并购,之后又被Osmetech Inc.于2003年并购。
(译者注: 2007年正式成立OPTI Medical Systems Inc.)
OPTI 测试片
用于OPTI仪器上的传感器被视为一次性测试片的一部分。图4(下方)展示了带有6个极点的测试片,该测试片通过荧光测量pH, PCO2,PO2, Na+ , K+ 和Ca2+。还有一些测试片可测量Cl-, 葡萄糖和尿素。 另外PO2传感器可提供全血的测量,并且通过3个波长的反射测量氧饱和度。血液被吸入测试片以后,其上的极点会迅速地将液体成分透过隔离层分散到传感器层。隔离层的目的就是阻止潜在的干扰物和周围的光线进入传感器。

图4 OPTI CCA仪器图片(左上方)、一次性测试片(右上方)、传感器薄膜(左下方)以及传感器盘(右下方)
pH和PCO2的测量
对于pH的测量,血液中氢离子与固定在传感层面上的pH敏感荧光指示染料相结合。 指示剂染料(HPTS)存在两种状态:质子化的和去质子化的,周围环境中的pH决定其相关数量(与血液样本平衡)。指示剂染料去质子化形式在水环境中发出荧光;但质子化形式不发出荧光,因此pH越低(氢离子浓度越高),质子化形式的比例就越高,荧光性就越低。这是一个可逆的以平衡为基础的结合过程,因此pH越高,荧光性就越强。
PCO2 极点是改良的pH极点,使用相同的指示剂染料但是有薄膜覆盖在传感层面上。薄膜阻挡了氢离子以及其他离子进入传感器的通道,但是却允许二氧化碳通过,在此二氧化碳形成碳酸,增强了局部氢离子浓度(pH减少)并且减弱了荧光性。因此增加的二氧化碳分压与低荧光结合在一起,降低的二氧化碳分压与高荧光结合在一起。这种间接测量pH的方法叫Severinghaus construction,并且这种方法运用在所有常规血气分析仪以及电化学pH电极上。
氧的测量
结合在测量系统上的氧极点用来计算氧饱和度和总血红蛋白。氧迅速扩散到传感器中与一个固定的染色分子相互作用。该染色分子是与氧相互作用的,在传感器中将会终止或减少染色分子的荧光。氧分压(PO2)和荧光强度的关系是由Stern-Volmer方程式决定的,即(I0/I=1+KPO2)。其中,当氧气为 0 托时,I0被视为最大强度,K是与氧分散比例和衰减横截面相关的Stern-Volmer衰减常量。该关系式是可逆的,如二氧化碳一样,导致氧分压越高荧光强度越弱。
总血红蛋白和氧饱和度的测量
测量系统中一个重要的组件就是位于PO2极点顶端的粉红反光覆膜。从一个LED和两个二极管发出的红外光直接照射到PO2极点非溶解的血液上。光被部分地吸收,另外一部分与血红素浓度成比例被红细胞反射。血红素水平低时,未被吸收的光照射粉红色覆膜,通过血液时再次被反射回去。一定比例的反射光存在于测试片的顶端,并且被仪器中的检测器来测量。结合两个红外波段和红色波长的读数,有可能获得测量两种血色素即含氧和脱氧血红素的最佳测量方法。
这些的总和相当于总血红蛋白的含量,氧基血红素的比例作为含氧和脱氧血红素的百分比就是氧饱和度。红细胞聚合测量的敏感度通过在测量之前维持高剪切力而降到最低。
常见阳离子电解质的测量
前面已经讨论了钠、钾和钙的极点3。它们的测量方法与以上描述的电极测量方法类似,都是使用离子选择识别元件,但是它们的离子载体相连的是荧光染料而不是电极,而且被定义为荧光离子载体。增加的离子浓度致使绑定在离子载体上的离子数量增加,这就使得荧光强度增强。正如前面提到的无需使用参比电极,但是一些离子确实存在很小的pH敏感度,这种情况可以在OPTI仪器测量pH时得以补偿。这些极点的主要元件是图5所示的荧光离子载体。
设计原则是基于光致电子转移(PET)。那些荧光离子载体非常成功地证明,作为直接的荧光阳离子传感分子,利用可转换的分子自淬灭机制和PET机制结合4。每个传感层包含固定的荧光离子载体并且附在透明的聚酯纤维箔顶端。传感层被一层黑色的亲水覆膜覆盖,使样本内部的光学干扰物和传感层分开。传感和覆膜层都是水凝胶的,允许离子通过传感器时自由快速地扩散,并且在测量时间内限制光学干扰血液成份的通道。三个荧光例子载体被合成一个活性连接器,以在不损失离子载体和荧光团功能的前提下完成亲水聚合物的共价固定。与水溶液或水相血液接触,三个荧光离子载体的离子载体部分与钠、钾和钙进行可逆性结合, 各自的离散常数分别为119mmol L-1, 17mmol L-1, 1.09mmol L-1,在37摄氏度的中性水溶液中,离子强度为pH 7.4和160mmol L-1。 所有这三种都使用四氨基萘作为荧光团, 比水解和光降解更稳定,显示了以消光系数产品和荧光定量产量为特征的强荧光性,并且使用蓝色的LED时更易激发。阳离子和每个离子载体部分的可逆性结合引起了相邻的四氨基萘荧光团经过PET时绿荧光的增强。不像大多数离子选择测量机制,该结合和信号转换发生在亲水环境中。三个新的荧光离子载体满足了系统要求的选择性、敏感度和光谱可达性。
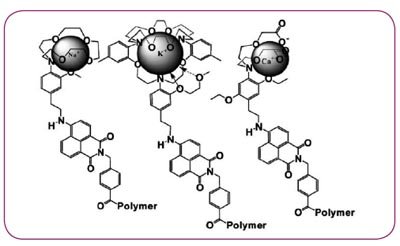
图5 钠、钾和钙荧光离子载体的结构
氯的测量
氯极点的构成是由基于吖啶酯的氯敏感指示剂被光敏化固定在亲水聚合物上。血液中的氯分散到传感器中阻塞并减弱的染料的荧光性。碰撞阻塞机制就像控制上述的氧传感器,氯和荧光强度之间的关系是以Stern-Volmer方程为特征的。该关系式是成反比例的,就像二氧化碳和氧气,氯的浓度越高导致荧光强度越弱。
OPTI仪器
OPTI分析仪内的测量系统的主要组成部分在图4中也有显示。发光二极管为极点提供了激发能量,激光器二极管用在基于反射的血氧定量法测量上。LED灯光通过分色光束分离器只是进入传感器。传感器的荧光通过分色光束分离器和过滤器返回,从而来分离出特殊的波长。然后光敏二极管探测器转变可见光子到可测量的电流中。 在各参数接近中等生理分析物水平执行一点强度定标,一次性测试片可测量多达8个血液分析物,同批次测试片由一组条形码表示批号、定标值、失效数据。它们是用在便携式的分析仪上,分析仪将其加热至37℃,利用光学过程6个蓝色的荧光LED执行自动定标,且自动吸入和测量来自注射器或毛细管的120μl的血液或血清样本。吸入后的测量少于60秒,含吸入和定标时间在内,总周期大约150秒。荧光离子载体有充足的水解稳定性,可以在8个月的室温潮湿环境中存储,且保持定标反应特征。
一次性测试片的生产
由于荧光极简单的延展面,无需电连接器和参比电极,荧光电极方便生产。 将它们准备作为复合层或含传感层的铝箔,夹在上光隔离层和下光传导黏合层之间。单个的传感器和荧光盘被冲压且插入一次性塑料测试片中。后者为两半的注射模具,当荧光盘插入后,使用超声波焊接在一起才形成了最终的测试片。
荧光电极生产过程中的关键部分是其工厂定标。一批荧光电极的典型定标曲线是通过测量六个不同分析物水平的荧光强度而得到的。回应是符合多项式曲线的,当测试片放置于仪器中时,输入测试片条形码的多参数也就输入到了仪器软件中。使用之前,工厂定标使用精度缓冲液和气体混合物检测一次。OPTI也使用运行时间诊断和额外的电子质控程序来检测仪器最佳运行时的光学、应用流体学、加热和电子学。以上特征及事实说明,除气瓶之外,OPTI测量系统无需试剂,这表现了比电化学系统的极大优势。光学传感器本身比电化学的类似产品有更小的复杂性,如上面提到的,更少的宏观组件、无需参比传感器、没有表面污染的生物蛋白以及无可滤取的可塑剂或其他化学产品。更少出错的元件,使得传感器技术更加牢固,并且系统能够在无冲洗或无定标的情况下,重复或连续检测全血。
临床性能
以荧光电极为基础的系统,其临床性能特征是通过4个生产批号的528个测试片为样本在4个地点的测量而得到的。与用在现代电极为基础的全血分析仪上的日常精确度和准确性相比,电解质测量的临床性能表现了更强的精确度和相同的准确性。表2显示了典型的20天研究精确度(1SD),其使用了安瓿控制原料±0.4 mmol L-1的钠、±0.025 mmol L-1的钾、±0.011 mmol L-1 的钙。研究准确性在可报告范围内:100-180 mmol L-1范围内钠占1.4%,在0.8-10 mmol L-1范围内,钾占2.2%,在0.2-3 mmol L-1范围内,钙占2.4%。报告的电解质值与pH和一般干扰物无关。由于血块、气泡、测试片定标错误、用户错误以及外露层等等,在含多批号测试片和多个不熟练的用户多与500个测量的过程中,要求重复测量的问题发生率小于1%。图6显示了OPTI CCA K+与台式参比仪器的典型相关性。
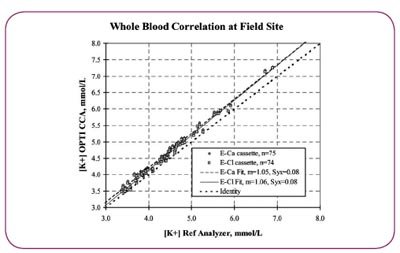
图6 OPTI CCA与其他仪器的相关性

表 2 20天客户精确度(场地)材料:安瓿液体控制
总结
传感器是医疗诊断分析仪的基础,新传感器技术的发展以满足重症监护日益显现的需求。没有一种传感器技术可以满足所有的需求。尽管微电极厚膜电极系列已被广泛地应用在包含频繁定标的大型台式分析仪上,光学传感器为床旁或病人检测等便携式应用的一次性传感器提供了引人注目的、稳定以及经济的选择。在光学传感器早期,其内在的稳定性、简单性以及经济性等优势还没有完全地在医疗诊断系统中开发出来。多亏新的主客体互动、光学材料以及实际电信元件的新发展,使用光学传感器的医学系统期望有一个快速的发展。
致谢
作者非常感谢与Marc J. P. Leiner 、Otto S. Wolfbeis 教授、A. P. de Silva 教授的讨论与合作,以及我们与AVL, Roche 和Osmetech的大力合作。
James K公司. Tusa and Huarui He*
Osmetech Inc, 235 Hembree Park Drive, Roswell, GA 30076, USA |